Médico especialista do artigo
Novas publicações
Síndrome de Goodpasture: Causas, Sintomas, Diagnóstico, Tratamento
Última revisão: 23.04.2024

Todo o conteúdo do iLive é medicamente revisado ou verificado pelos fatos para garantir o máximo de precisão factual possível.
Temos diretrizes rigorosas de fornecimento e vinculamos apenas sites de mídia respeitáveis, instituições de pesquisa acadêmica e, sempre que possível, estudos médicos revisados por pares. Observe que os números entre parênteses ([1], [2], etc.) são links clicáveis para esses estudos.
Se você achar que algum dos nossos conteúdos é impreciso, desatualizado ou questionável, selecione-o e pressione Ctrl + Enter.
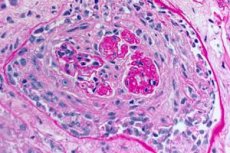
A síndrome de Goodpasture é uma síndrome autoimune que inclui hemorragia pulmonar alveolar e glomerulonefrite causada por anticorpos anti-GBM circulantes. A síndrome de Goodpasture geralmente se desenvolve em pessoas com predisposição hereditária, que fumam cigarros, mas possíveis fatores adicionais são a inalação de hidrocarbonetos e infecções virais do trato respiratório. Os sintomas da síndrome de Goodpasture incluem falta de ar, tosse, fadiga, hemoptise e / ou hematúria. A síndrome de Goodpasture é suspeita em pacientes com hemoptise ou hematúria e é confirmada pela presença de anticorpos anti-GVM no sangue. Tratamento A síndrome de Goodpacers inclui plasmaferese, glicocorticóides e imunossupressores, como a ciclofosfamida. O prognóstico é favorável se o tratamento for iniciado antes do desenvolvimento de insuficiência respiratória ou renal.
A Síndrome de Goodpasture foi descrita pela primeira vez por Goodpasther em 1919. A síndrome Goodpasture é uma combinação de glomerulonefrite e hemorragia alveolar na presença de anticorpos anti-GVM. A síndrome Goodpasture é mais frequentemente manifestada por uma combinação de hemorragia alveolar difusa e glomerulonefrite, mas às vezes causa glomerulonefrite isolada (10-20%) ou danos pulmonares (10%). Os homens estão doentes mais frequentemente do que as mulheres.
O que causa síndrome de Goodpasture?
A causa da doença não está exatamente estabelecida. A predisposição genética à síndrome de Goodpasture é suposta, seu marcador é considerado a presença de HLA-DRW2. Existe um ponto de vista sobre o possível papel da infecção por vírus transferida (vírus da hepatite A e outras doenças virais), riscos de produção, drogas (especialmente D-penicilamina).
A base da patogênese da síndrome de Goodpasture é a formação de autoanticorpos nas membranas basais dos capilares dos glomérulos dos rins e alvéolos. Estes anticorpos pertencem à classe de IgG, eles se ligam aos anticorpos das membranas basais na presença do componente C3 do complemento, seguido pelo desenvolvimento de inflamação imune dos rins e alvéolos pulmonares.
Anti-GVM-anticorpos dirigidos contra os não colagenoso (NC1) cadeias OS domínio de colagénio de tipo IV, que é a concentração mais elevada é na membrana basal dos capilares renais e pulmonares. A exposição a factores ambientais - fumar, virais ARI e bicarbonato de inalação lamas (mais frequentemente) - e, menos frequentemente, pneumonia activa de apresentação de antigénio capilares alveolares anticorpos em indivíduos que circulam com uma predisposição hereditária (na maioria das vezes transportadores de HLA-DRwl5, - DRB1 - DR4 e ). Circulating anti-GVM-anticorpos ligam-se à membrana basal, fixar o complemento e induzir a resposta inflamatória celular, resultando no desenvolvimento de glomerulonefrite, e / ou kapillyarita pulmonar.
Provavelmente, há uma generalidade definitiva de auto-antígenos da membrana basal dos capilares dos glomérulos dos rins e alvéolos. O autoantígeno é formado sob a influência do efeito prejudicial do fator etiológico. Um fator etiológico desconhecido dano e modifica a estrutura das membranas basais dos rins e pulmões. A excreção dos produtos de degradação formada das membranas basais dos glomérulos dos rins durante a lesão diminui e diminui, o que naturalmente cria os pré-requisitos para o desenvolvimento de lesões auto-imunes dos rins e pulmões. Ainda é completamente desconhecido qual componente da membrana basal se torna um auto-antígeno. No presente, presume-se que este é um componente estrutural interno da membrana basal do glomérulo do colágeno a3 do rim de tipo 4.
Os complexos imunes formados são depositados ao longo das membranas basais dos capilares glomerulares, o que leva ao desenvolvimento de um processo imuno-inflamatório no glomérulo renal (glomerulonefrite) e alvéolos (alveolite). As principais células envolvidas no desenvolvimento desta inflamação imune são linfócitos T, monócitos, endoteliocitos, leucócitos polimorfonucleares, macrófagos alveolares. A interação entre eles é fornecida por mediadores moleculares, citocinas (fatores de crescimento - plaquetas, insulina, b-transformação, interleucina-1, fator de necrose tumoral, etc.). Um papel importante no desenvolvimento da inflamação imune é desempenhado pelos metabólitos do ácido araquidônico, radicais livres de oxigênio, enzimas proteolíticas, moléculas de adesão.
No desenvolvimento da alveolite na síndrome de Goodpasture, a ativação de macrófagos alveolares é de grande importância. No estado ativado, eles liberam cerca de 40 citocinas. As citocinas do grupo I (quimiotaxinas, leucotrienos, interleucina-8) aumentam o fluxo de leucócitos polimorfonucleares para os pulmões. As citocinas do grupo II (fatores de crescimento - plaquetas, macrófagos) promovem o movimento dos fibroblastos para os pulmões. Os macrófagos alveolares também produzem formas ativas de oxigênio, proteases que danificam o tecido pulmonar.
Patomorfologia da síndrome de Goodpasture
As principais manifestações patomorfológicas da síndrome de Goodpasture são:
- a lesão primária da cama microcirculatória dos rins e pulmões. Nos pulmões há uma imagem de vênulas, arteriolitos, capilarites com destruição e proliferação marcadas; A derrota dos capilares é observada principalmente em septos interalveolares, a alveolite com exsudato hemorrágico se desenvolve nos alvéolos. O dano renal é caracterizado pelo desenvolvimento de glomerulonefrite proliferativa extracapilar seguida pela formação de hialinose e fibrose, o que leva ao desenvolvimento de insuficiência renal;
- hemorragia intra-alveolar grave;
- desenvolvimento de hemossiderose dos pulmões e pneumosclerose de severidade variável, como resultado da evolução da alveolite.
Sintomas da síndrome de Goodpasture
A doença geralmente começa com manifestações clínicas de patologia pulmonar. A hemoptise é o sintoma mais proeminente; no entanto, a hemoptise pode estar ausente na presença de manifestações hemorrágicas, e o paciente só pode detectar alterações infiltrativas na radiografia de tórax ou infiltrado e síndrome de dificuldade respiratória e / ou insuficiência. Muitas vezes, desenvolve falta de ar (principalmente com esforço físico), tosse, mal-estar, deficiência, dor no peito, febre e perda de peso. Até 40% dos pacientes apresentam macrohematuria, embora a hemorragia pulmonar possa preceder as manifestações renais durante semanas e anos.
A disnea pode aumentar durante a hemoptise. As preocupações também são fraqueza, deficiência.
Os sintomas da síndrome de Goodpasture variam em um longo período de tempo, desde pulmões puros até auscultação, crepitação e sibilos secos. Alguns pacientes experimentam edema periférico e palidez devido à anemia.
Ao examinar, a atenção é desenhada para a palidez da pele, a cianose das mucosas, a pastoral ou o edema pronunciado do rosto, a redução da força muscular, a perda de peso corporal. A temperatura corporal geralmente é aumentada para dígitos febris.
Com a percussão dos pulmões, o acortamento do som de percussão sobre os vastos focos de hemorragia pulmonar pode ser determinado, mas isso é raro, geralmente não há alteração no som de percussão.
Um sinal auscultivo característico da síndrome de Goodpasture é o sibilo seco e úmido, o número deles aumenta significativamente durante ou após a hemoptise.
Ao examinar o sistema cardiovascular, a hipertensão arterial é detectada, é possível aumentar a borda da tontura relativa do coração à esquerda, tons de coração abafados, ruído sistólico silencioso, com o desenvolvimento de insuficiência renal grave aparece ruído de fricção pericárdica. Com dano renal progressivo em um fundo de hipertensão arterial significativa, é possível desenvolver insuficiência ventricular esquerda aguda com imagem de asma cardíaca e edema pulmonar. Geralmente, essa situação se desenvolve no estágio terminal da doença.
Em regra, o dano renal manifesta-se mais tarde, após um certo tempo após o desenvolvimento de sintomas pulmonares. Os sinais clínicos característicos de patologia renal são hematúria (às vezes macrohematuria), insuficiência renal progressiva, oligoanúria, hipertensão arterial.
Em 10-15% dos casos, a síndrome de Goodpasture começa com sinais clínicos de patologia renal - há uma clínica de glomerulonefrite (oligúria, edema, hipertensão arterial, palidez pronunciada) e, em seguida, sinais de lesão pulmonar se juntam. Muitos pacientes podem ter mialgia, artralgia.
Independentemente das opções, a síndrome de Goodpasture na maioria dos casos é difícil, a doença progride de forma constante, desenvolve-se insuficiência pulmonar e renal grave. A expectativa de vida dos pacientes desde o início da doença varia de vários meses a 1-3 anos. Na maioria das vezes, os pacientes morrem de urêmia ou hemorragia pulmonar.
O que está incomodando você?
Diagnóstico da síndrome de Goodpasture
O diagnóstico da síndrome de Goodpasture requer a detecção de anticorpos anti-GVM séricos por imunofluorescência indireta ou, se possível, por meio de ensaio imunoenzimático direto (ELISA) com NC-1 a3 recombinante humano. Outros testes sorológicos, como o teste de anticorpos anti-nucleares (ANA), são usados para detectar SLE, anti-reptolissina-O-titulo para a detecção de glomerulonefrite pós-estreptocócica, que pode ser a causa de muitos casos de síndrome pulmonar-renal. A ANCA é positiva (em padrões periféricos) em 25% dos casos de síndrome de Goodpasture. Na presença de glomerulonefrite (hematúria, proteinúria, lodo de eritrócitos na análise de urina e / ou insuficiência renal), uma biópsia de rim pode ser administrada. A glomerulonefrite necrosante segmentar focal rapidamente progressiva com um curso progressivo é detectada com biópsia na síndrome de Goodpasture e todas as outras causas da síndrome pulmonar-renal. A coloração por imunofluorescência do tecido renal ou pulmonar revela classicamente a deposição linear de IgG ao longo de capilares glomerulares ou alveolares. Isso também ocorre em glóbulos diabéticos e glomerulonefrite fibrilar, uma doença rara que causa síndrome pulmonar-rim, mas a fixação de anticorpos GBM nestas doenças não é específica.
Estudos de função pulmonar e lavagem broncoalveolar não são diagnósticos na síndrome de Goodpasture, mas podem ser usados para confirmar a presença de hemorragia alveolar difusa em pacientes com glomerulonefrite e infiltrados pulmonares, mas sem hemoptise. O líquido de lavagem, que permanece hemorrágico após a lavagem repetida, permite confirmar uma síndrome hemorrágica difusa, especialmente com a diminuição concomitante no hematócrito.
 [3],
[3],
Diagnóstico laboratorial da síndrome de Goodpasture
- Teste de sangue geral. Característica de deficiência de ferro, anemia hipocrômica, hipocromia, anisocitose, poicilocitose de eritrócitos. Há também leucocitose, uma mudança da fórmula de leucócitos para a esquerda, um aumento significativo na ESR.
- Análise geral da urina. Na urina, uma proteína é detectada (o grau de proteinúria pode ser significativo), cilindros (granular, hialino, eritrócitos), eritrócitos (pode ser macrohematuria). À medida que a progressão da insuficiência renal crônica diminui, a densidade relativa da urina, na amostra, Zimnitsky desenvolve iso-hipertenção.
- Teste de sangue bioquímico. Existe um aumento nos níveis de ureia, creatinina, haptoglobina, seromucóide, a2 e gama de globulina no sangue , uma diminuição no teor de ferro.
- Pesquisa imunológica. Pode haver uma diminuição no número de supressores de linfócitos T, revelando-se complexos imunes circulantes. Anticorpos à membrana basal dos capilares dos glomérulos e alvéolos são detectados por imunofluorescência indireta ou por radioimunoensaio.
- Análise do escarro. Há uma grande quantidade de glóbulos vermelhos no escarro, hemosiderina, siderófagos são encontrados.
Diagnóstico instrumental da síndrome de Goodpasture
- Análise de raios-X dos pulmões. Os sinais radiográficos característicos são infiltrados pulmonares na área basal, espalhando-se para as secções inferior e média dos pulmões, bem como infiltrados bilaterais bilaterais simétricos progressivos.
- Exame da função de respiração externa. A espirrografia revela um tipo restritivo de insuficiência respiratória (uma diminuição no GEL), à medida que a doença progride, é adicionado um tipo obstrutivo de insuficiência respiratória (redução do VEF1, índice Tiffno).
- ECG. Existem sinais de distrofia miocárdica pronunciada de gênese anêmica e hipóxica (uma diminuição da amplitude da onda T e do intervalo ST em muitas derivações, mais freqüentemente na região torácica esquerda). Com hipertensão arterial grave, há sinais de hipertrofia miocárdica do ventrículo esquerdo.
- Investigação da composição de gás do sangue. A hipoxemia arterial é revelada.
- Investigação de amostras de biópsia de pulmão e rim. Uma biópsia do tecido pulmonar (biópsia aberta) e rins é feita para a verificação final do diagnóstico, se for impossível diagnosticar com precisão a doença com métodos não invasivos. O exame histológico e imunológico de espécimes de biópsia é realizado. Típico para a síndrome de Goodpasture são os seguintes sintomas:
- presença de sinais morfológicos de glomerulonefrite (na maioria das vezes extracapilar), alveolite hemorrágica, hemosiderose e fibrose intersticial;
- detecção pelo método de imunofluorescência de deposição linear de componentes de complemento de IgG e C3 em membranas basais de alvéolos pulmonares e glomérulos renais.
Critérios diagnósticos para síndrome de Goodpasture
Ao fazer o diagnóstico da síndrome de Goodpasture, é aconselhável usar os seguintes critérios.
- A combinação de patologia pulmonar e patologia renal, i.e. Hemoptise (freqüentemente hemorragia pulmonar), dispnéia e sintomas de glomerulonefrite.
- Um curso progressivo da doença com o desenvolvimento de insuficiência respiratória e renal.
- Desenvolvimento de anemia ferropriva.
- Identificação de múltiplos infiltrados bilaterais semelhantes a nuvens no exame de raios X dos pulmões no contexto de uma deformação da rede do padrão pulmonar.
- Detecção no sangue de títulos elevados de anticorpos circulantes para a membrana basal de glomérulos e alvéolos renais.
- Detecção de depósitos lineares dos componentes do complemento IgG e C3 nas membranas basais dos capilares e alvéolos glomerulares.
- Ausência de outras manifestações sistêmicas (exceto pulmonares e renais).
Diagnóstico diferencial da síndrome de Goodpasture
A síndrome de Goodpasture deve ser diferenciada com uma série de doenças manifestadas por hemoptise ou hemorragia pulmonar. É necessário excluir doenças oncológicas de brônquios e pulmões, tuberculose, abscessos pulmonares, bronquiectasias, doenças cardíacas e vasculares (levando a estagnação e hipertensão no pequeno círculo), vasculite sistêmica, diátese hemorrágica.
O programa de inspeção na síndrome de Goodpasture
- Testes de sangue comuns, testes de urina.
- Análise bioquímica de sangue: determinação do conteúdo das frações protéicas e protéicas totais, creatinina e ureia, transaminases, seromucóides, haptoglobina, fibrina, ferro.
- Análise do escarro: exame citológico, definição de siderófagos.
- Estudos imunológicos: determinação do conteúdo de linfócitos B e T, subpopulações de linfócitos T, imunoglobulinas, complexos imunes circulantes, anticorpos contra as membranas basais dos glomérulos dos rins e alvéolos.
- Análise de raios-X dos pulmões.
- ECG.
- Spirography.
- Investigação de amostras de biópsia de pulmão e rim.
Quais testes são necessários?
Tratamento da síndrome de Goodpasture
Síndroma de Goodpasture tratamento incluem diariamente ou a cada dois dias plasmaferese realizada durante 2-3 semanas (plazmozameschenie 4 L) para remover-GBM-anticorpo aHTH em combinação com a administração intravenosa de glucocorticoides (metilprednisolona geralmente um g durante pelo menos 20 minutos por dia, três vezes com prednisolona 1 mg / kg de peso corporal diariamente) e ciclofosfamida (2 mg / kg uma vez por dia) por 6-12 meses para prevenir a formação de novos anticorpos. A terapia pode ser reduzida quando a melhora da função pulmonar e renal cessa. A mortalidade a longo prazo está associada ao grau de insuficiência renal no início da doença; Os pacientes que necessitaram de diálise no início, bem como aqueles que tiveram mais de 50% de nefronas com crescentes em biópsia, têm um tempo de sobrevivência de menos de 2 anos e muitas vezes requerem diálise se o transplante renal não for realizado. A hemoptise pode ser um bom sinal prognóstico, porque leva a uma detecção precoce da doença; Uma minoria de pacientes que são ANCA-positivos responde melhor ao tratamento da síndrome de Goodpasture. A recaída ocorre em uma pequena porcentagem de casos e está associada à continuação do tabagismo e à infecção do trato respiratório. Em pacientes com fase terminal de insuficiência renal submetidos a transplante renal, a doença pode se repetir no transplante.
Qual é a síndrome de Goodpasture?
A síndrome de Goodpasture geralmente progride rapidamente e pode ser fatal se o diagnóstico rápido e o tratamento da síndrome de Goodpasture não forem realizados; O prognóstico é favorável quando o tratamento começa antes do desenvolvimento de insuficiência respiratória ou renal.
A sobrevivência imediata no momento da hemorragia pulmonar e insuficiência respiratória está associada à garantia da permeabilidade das vias aéreas; O som endotraqueal e a ventilação artificial são recomendados para pacientes com níveis limítrofes de gases no sangue arterial e ameaça de insuficiência respiratória.

