Médico especialista do artigo
Novas publicações
Malária
Última revisão: 04.07.2025

Todo o conteúdo do iLive é medicamente revisado ou verificado pelos fatos para garantir o máximo de precisão factual possível.
Temos diretrizes rigorosas de fornecimento e vinculamos apenas sites de mídia respeitáveis, instituições de pesquisa acadêmica e, sempre que possível, estudos médicos revisados por pares. Observe que os números entre parênteses ([1], [2], etc.) são links clicáveis para esses estudos.
Se você achar que algum dos nossos conteúdos é impreciso, desatualizado ou questionável, selecione-o e pressione Ctrl + Enter.
A malária (malária em inglês; paludisme em francês) é uma doença protozoária transmissível antroponótica aguda com um mecanismo de infecção transmissível, caracterizada por sintomas pronunciados de intoxicação, um curso cíclico com ataques alternados de febre e períodos de apirexia, aumento do baço e do fígado, desenvolvimento de anemia hemolítica com curso progressivo e recidivas da doença.
Epidemiologia
A fonte do agente infeccioso é uma pessoa doente ou um portador do parasita cujo sangue contém gametócitos. A malária é uma infecção transmissível transmitida pela picada de mosquito. Gametócitos de P. vivax, P. ovale e P. malariae são encontrados no sangue nos primeiros dias da doença; seu número aumenta após vários ciclos de esquizogonia eritrocítica. Quando infectado com P. falciparum, uma pessoa se torna uma fonte de infecção 10 a 12 dias após o início da parasitemia e pode permanecer assim por 2 meses ou mais.
Com a malária, vários mecanismos de transmissão da infecção são possíveis:
Mecanismo de transmissão (picada de mosquito)
Este mecanismo é o principal, garantindo a existência dos plasmódios como espécie biológica. A fonte de infecção é uma pessoa (doente de malária ou portadora do parasita), em cujo sangue existem gametócitos maduros (células reprodutivas masculinas e femininas do parasita). Os portadores da malária são apenas mosquitos fêmeas do gênero Anopheles.
No estômago do mosquito, por onde os gametócitos masculinos e femininos dentro dos eritrócitos entram juntamente com o sangue, ocorre sua posterior maturação (após a lise dos eritrócitos), fusão e divisão múltipla, com a formação de esporozoítos, que se acumulam nas glândulas salivares do mosquito. Formas assexuadas do parasita (trofozoítos, esquizontes), ao entrarem no estômago do mosquito, morrem.
Assim, no corpo humano, ocorre uma via assexuada de desenvolvimento do parasita (esquizogonia) com a formação e acúmulo de gametócitos, e no corpo do mosquito, ocorre uma via sexual (esporogonia), a fusão dos gametócitos masculinos e femininos com seu posterior desenvolvimento e a formação de esporozoítos.
 [ 4 ], [ 5 ], [ 6 ], [ 7 ], [ 8 ], [ 9 ]
[ 4 ], [ 5 ], [ 6 ], [ 7 ], [ 8 ], [ 9 ]
Mecanismo de transmissão vertical
Mecanismo de transmissão vertical (da mãe para o feto) ou da mãe para o recém-nascido (durante o parto - mecanismo parenteral). Na transmissão vertical, o feto raramente é infectado pela placenta. Mais frequentemente, a infecção ocorre durante o parto, quando uma certa quantidade de sangue materno entra na corrente sanguínea do recém-nascido, em cujos eritrócitos existem formas assexuadas do parasita.
Mecanismo parenteral de transmissão
O mecanismo parenteral de infecção leva ao desenvolvimento da chamada malária esquizontes. Ela ocorre durante transfusões de sangue ou, menos frequentemente, durante violações da assepsia durante injeções (por exemplo, entre dependentes químicos que usam a mesma seringa). Em caso de infecção durante transfusão de sangue, a fonte de infecção é um doador-parasita portador, frequentemente com parasitemia sublatêntica (o número de parasitas é inferior a cinco em um μl de sangue). Portanto, em regiões do mundo endêmicas para malária, é necessário utilizar, juntamente com métodos parasitológicos (detecção do parasita em preparações de gotas espessas e esfregaços sanguíneos), métodos sorológicos (imunológicos) de diagnóstico laboratorial da malária (RNIF, ELISA, etc.) para controlar o sangue doado. Considerando que, na infecção parenteral, geralmente apenas alguns parasitas são introduzidos (especialmente com injeções), o período de incubação pode ser estendido para 3 meses (na infecção maciça, o período de incubação, ao contrário, pode ser muito curto - vários dias), o que é importante saber ao diagnosticar a malária em pacientes submetidos a cirurgia e viciados em drogas.
Condições de propagação da malária
Para que a malária se espalhe em uma determinada região (país, território, área), são necessárias as seguintes condições:
- Fonte de infecção (um paciente com malária ou um portador do parasita).
- A presença de um vetor eficaz (mosquitos do gênero Anopheles). A suscetibilidade aos parasitas da malária é a principal característica de uma espécie específica de mosquito do gênero Anopheles. O número de mosquitos do gênero Anopheles entre populações de outras espécies não é tão alto quanto o de mosquitos não relacionados à malária, e raramente causam sérios danos com suas picadas. No entanto, mesmo espécies pequenas, em outras circunstâncias favoráveis (a proximidade de criadouros de mosquitos a habitações humanas), podem desempenhar um papel bastante significativo. Mais de 70 espécies de mosquitos do gênero Anopheles (de mais de 200 espécies conhecidas) podem atuar como vetores eficazes da malária.
- Condições climáticas favoráveis: temperatura média diária do ar acima de 16 °C e presença de criadouros para mosquitos: corpos d'água, reservatórios, estruturas de irrigação, etc. A temperatura média diária mínima do ar necessária para o desenvolvimento no corpo do mosquito Pl. vivax é de 16 °C, para Pl. falciparum - 18 °C, em temperaturas mais baixas a esporogonia não ocorre. A duração da esporogonia é menor quanto mais alta a temperatura (até certo ponto, já que uma temperatura média diária de 30 °C ou mais é desfavorável à esporogonia). Em uma temperatura média diária ideal (25-26 °C), a esporogonia em Pl. vivax leva de 8 a 9 dias, em Pl. falciparum - 10 a 11 dias.
Toda a área de distribuição da malária no globo (entre 45° N e 40° S a 64° N e 45° S em anos diferentes) é ocupada pela malária vivax. As áreas de malária falciparum e malariae malariae são um pouco menores devido à temperatura mais alta necessária para a esporogonia eficaz; a área de malária ovale está localizada em duas regiões que não estão territorialmente conectadas entre si: a África tropical e os estados da parte ocidental do Oceano Pacífico (Indonésia, Vietnã, Filipinas, Nova Guiné, etc.). Em países montanhosos, focos de malária podem se formar em altitudes de até 1.000 m na zona climática temperada e até 1.500-2.500 m na zona subtropical e tropical, com focos apenas de malária vivax ocorrendo em altas altitudes (1.000-1.500 m e mais).
A malária é caracterizada por uma sazonalidade pronunciada. Em climas temperados e subtropicais, a estação da malária é dividida em períodos de infecção efetiva do mosquito, transmissão da infecção e manifestações em massa da doença. O início do período de infecção efetiva do mosquito (na presença de uma fonte de infecção - pacientes, portadores do parasita) coincide com o momento de um aumento estável na temperatura média diária para 16 °C. O início do período de transmissão está associado à conclusão da esporogonia no corpo do mosquito, que depende das temperaturas médias diárias específicas de um determinado ano. Na região de Moscou, o período de transmissão da malária vivax pode atingir 1,5 a 2 meses ou mais, até as primeiras geadas de outono. Os limites do período de manifestações em massa são menos definidos. Em focos onde apenas a malária de três dias é transmitida, a morbidade em massa pode começar muito antes do início do período de transmissão. Os casos observados são manifestações primárias de malária vivax com longo período de incubação (3-10 meses) devido à infecção na estação anterior e à preservação de hipnozoítos no fígado (sem manifestações primárias com curto período de incubação), bem como recidivas exoeritrocíticas distantes (após uma série de ataques de malária com curto período de incubação na estação anterior, sem terapia anti-recidiva adequada).
A suscetibilidade à malária é universal. O resultado da infecção após a entrada do patógeno na corrente sanguínea e o curso clínico da doença são determinados pelo estado imunológico individual, pela atividade de fatores de resistência inatos não específicos, pela intensidade da imunidade pós-infecção e, no caso de recém-nascidos, pelo nível de anticorpos específicos da classe G recebidos da mãe. A exceção são os povos indígenas da África Ocidental e da Nova Guiné, que são majoritariamente imunes à infecção por Pl. vivax, o que está associado à ausência, geneticamente determinada, de isoantígenos eritrocitários do grupo Duffy, que atuam como receptores para merozoítos de Pl. vivax. Consequentemente, nessa região, os casos de infecção por malária vivax são observados significativamente menos frequentemente do que em outras regiões da África tropical.
Pessoas portadoras de hemoglobina anormal (talassemia, anemia falciforme, hemoglobina E, C, etc.), com anormalidades na estrutura do citoesqueleto eritrocitário (esferocitose hereditária, ovalocitose do sudeste, eliptocitose hereditária) ou com deficiência da enzima glicose-6-fosfato desidrogenase dos eritrócitos apresentam relativa resistência à infecção por todos os tipos de plasmódios. Em caso de infecção por malária, a doença é leve, o número de parasitas no sangue permanece relativamente baixo e os casos de progressão maligna (malária cerebral - falciparum) são praticamente inexistentes. Por outro lado, pessoas com deficiência de glicose-6-fosfato desidrogenase correm o risco de desenvolver hemólise aguda ao usar diversos medicamentos antimaláricos (primaquina, quinina, etc.). Os mecanismos de resistência natural a vários tipos de malária ainda são pouco conhecidos e continuam a ser estudados.
Os recém-nascidos também apresentam certa resistência à infecção por todas as formas de malária. Isso se deve a:
- a presença de imunidade passiva devido aos anticorpos da classe G recebidos pelo recém-nascido de uma mãe hiperimune (em áreas com alta incidência de malária);
- manter imunidade específica após o nascimento devido aos anticorpos da classe A recebidos pelo recém-nascido com o leite materno;
- a presença de hemoglobina fetal no recém-nascido, que é de pouca utilidade para alimentar o parasita da malária.
Após os primeiros três a seis meses de vida, os recém-nascidos apresentam um risco significativamente maior de desenvolver formas graves e malignas de malária falciparum (mudança de glóbulos vermelhos contendo hemoglobina fetal para glóbulos vermelhos contendo hemoglobina normal; transição para alimentação mista - ingestão de ácido para-aminobenzóico, necessário para o desenvolvimento do parasita, que está ausente no leite materno).
 [ 10 ], [ 11 ], [ 12 ], [ 13 ]
[ 10 ], [ 11 ], [ 12 ], [ 13 ]
Imunidade na malária
A imunidade à malária é não estéril, específica para cada espécie e cepa, instável e de curta duração. Para manter o nível protetor de anticorpos, é necessária a estimulação antigênica constante na forma de infecções recorrentes por malária. A imunidade contra Pl. malariae e Pl. vivax é estabelecida mais precocemente e mantida por mais tempo do que contra Pl. falciparum. A imunidade antimalárica inclui respostas celulares e humorais. Os processos imunológicos que estimulam a síntese de anticorpos começam com a fagocitose dos parasitas da malária pelos macrófagos. Isso se manifesta pela hiperplasia do sistema histiofagocítico do baço, fígado e medula óssea.
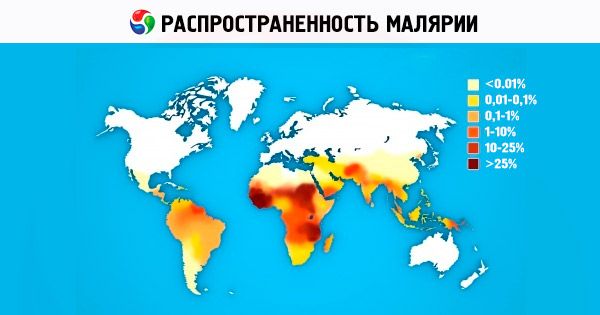
Prevalência da malária
Das quatro espécies de patógenos da malária humana, P. vivax é o mais comum no mundo. Nos subtrópicos e trópicos, os esporozoítos predominam no pool genético da população de P. vivax. Eles causam a doença após uma curta incubação (10-21 dias). No continente africano, P. vivax é constantemente encontrado nos países da África Oriental entre árabes, indianos, etíopes e europeus. Nos países da África Ocidental, que é povoada principalmente por representantes da raça negroide, P. vivax não é encontrado, o que é explicado pela imunidade inata geneticamente determinada dos negros africanos ao P. vivax [os eritrócitos não têm um receptor para merozoítos de P. vivax - isoantígenos Duffy (Fy d ou Fy b )]. O alcance de P. ovale é pequeno e consiste em duas partes. A parte principal, africana, ocupa a África tropical, da Gâmbia, no norte, ao Congo, no sul do continente. A segunda parte da distribuição abrange os países do Oceano Pacífico Ocidental e do Sudeste Asiático. A distribuição geográfica da malária tropical atinge 40° de latitude norte e 20° de latitude sul. O P. falciparum causa até 50% dos casos de malária no mundo. A malária de quatro dias é atualmente encontrada na África, em algumas áreas da América Central e do Sul e no Caribe. Sudeste Asiático.
A maioria das pessoas é suscetível à malária. A exceção é a população indígena da África Ocidental. As áreas hiperendêmicas da África tropical, onde predomina o P. falciparum, são caracterizadas por uma estrutura imunológica relativamente estável da população indígena:
- Crianças menores de 6 meses não adoecem devido à imunidade passiva recebida da mãe:
- A maioria das crianças de 6 a 24 meses está infectada com P. falciparum; a imunidade passiva diminuiu, a imunidade ativa ainda não se desenvolveu; este grupo tem a maior mortalidade por malária:
- Em crianças maiores de 2 anos, o P. falciparum é detectado com menor frequência, o curso da malária é atenuado em decorrência da imunidade adquirida e a intensidade da parasitemia diminui com a idade:
- Em adultos, o P. falciparum raramente é detectado devido à alta tensão imunológica; quando infectado, não há manifestações clínicas.
A malária tropical também é facilmente tolerada por portadores de hemoglobina S anormal (anemia falciforme) e pessoas com outras anormalidades geneticamente determinadas de hemoglobina e enzimas de glóbulos vermelhos (deficiência de G-6-PDH).
História da pesquisa sobre malária
O estudo da malária (uma das doenças humanas mais antigas) está inextricavelmente ligado à história da civilização humana. Supõe-se que a malária tenha começado a se espalhar na Terra (a partir da região africana do Mediterrâneo) há cerca de 10.000 anos, devido ao intenso desenvolvimento da agricultura, do comércio e da exploração de novas terras. Em antigos papiros egípcios, na literatura chinesa antiga e nos cânones da medicina indiana clássica (Ayurveda), descrições do quadro clínico e das epidemias de malária sobreviveram até hoje; mesmo então, suposições foram feitas sobre uma possível conexão entre o desenvolvimento da doença e picadas de mosquito. Mais tarde (séculos V-VI a.C.), médicos gregos antigos: Hipócrates, Herádoto e Empédocles descreveram o quadro clínico da malária em detalhes. Hipócrates é creditado por distinguir a malária do grupo de doenças febris: ele propôs distinguir 3 formas da doença: “cotidiana” (ataques diários), “terçã” (ataques em dias alternados) e “quartã” (ataques a cada 2 dias).
O início da era das descobertas científicas no estudo da malária está associado a 1640, quando o médico e conquistador espanhol Juan del Vego utilizou pela primeira vez uma infusão de casca de cinchona para tratar pacientes com malária, anteriormente usada pelos indígenas do Peru e do Equador como antipirético. O crédito pela denominação da doença "malária" (em italiano: "malaria" - ar ruim) cabe ao italiano Lancisi (1717), que associou a infecção de pessoas com malária por meio de vapores "venenosos" de pântanos. Em 1880, o médico francês A. Laveran, trabalhando na Argélia, descreveu em detalhes a morfologia do patógeno da malária. Em 1897, o médico militar inglês Ronald Ross, na Índia, estabeleceu o mecanismo de transmissão da malária.
Atualmente, a malária é um dos problemas de saúde mais graves para mais de 100 países na África, Ásia e América do Sul, cerca de metade da população mundial vive em risco de contrair malária. Quase todos os países da Europa e América do Norte registram anualmente centenas de casos importados de malária entre pessoas que chegam de regiões onde é disseminada, o número de casos da chamada malária de aeroporto está crescendo. Segundo a OMS, 200 a 250 milhões de pessoas no mundo adoecem com malária todos os anos, pelo menos 80% de todos os casos de malária são registrados em países africanos localizados ao sul do Saara. Todos os anos, 1 a 2 milhões de pessoas morrem de malária, principalmente crianças menores de 5 anos de idade. As perdas sociais e econômicas somente na África são estimadas em 2 bilhões de dólares americanos por ano. Desde 1998, sob os auspícios da OMS, do Banco Mundial e da UNICEF, um programa científico e prático (Iniciativa Roll Back Malaria) para o controle da malária (principalmente em países em desenvolvimento) foi implementado. O programa está previsto para durar entre 2010 e 2015. O desenvolvimento de uma vacina eficaz contra a malária está em andamento, mas isso levará pelo menos mais 10 a 15 anos. A busca, o desenvolvimento e o aprimoramento de medicamentos para o tratamento da malária são um dos programas prioritários da OMS, de diversas empresas farmacêuticas e de institutos de pesquisa em todo o mundo. Nos últimos anos, a Rússia tem registrado um aumento nos casos importados de malária, como resultado do aumento da migração e do desenvolvimento intensivo do turismo internacional.
Causas malária
O nome da doença "malária" na verdade generaliza quatro doenças protozoárias distintas causadas por quatro tipos de patógenos, respectivamente.
A malária é causada por parasitas pertencentes ao gênero Protozoa, classe Sporozoa, família Plasmodiidae e gênero Plasmodium. Quatro tipos do patógeno parasitam humanos: P. vivax, causador da malária de três dias; P. malariae, causador da malária de quatro dias; P. falciparum, causador da malária tropical; e P. ovale, causador da malária oval de três dias.
Patógenos da malária
Excitador |
Forma de malária (de acordo com a CID-10) |
Plasmodium (Laverania) falciparum |
Malária causada por Plasmodium falciparum (malária falciparum) |
Plasmodium (Plasmodium) vivax |
Malária causada por Plasmodium vivax (malária-vivax) |
Plasmodium (Plasmodium) ovale |
Malária causada por Plasmodium ovale (malária-ovale) |
Malária por Plasmodium (Plasmodium) |
Malária causada por Plasmodium malariae (malária-malariae) |
Na maioria das publicações nacionais (livros didáticos, manuais, livros de referência), os nomes anteriores das formas de malária são mantidos: malária tropical (malaria-falciparum), malária de três dias (malaria-vivax), malária oval (malaria-ovale) e malária de quatro dias (malaria-malariae).
Cada uma das quatro formas de malária é caracterizada por suas próprias características clínicas, patogênicas e epidemiológicas. O lugar mais importante é ocupado pela malária falciparum, responsável por 80 a 90% de todos os casos de malária no mundo, cujo agente causador pertence a um subgênero especial (Laverania). Somente a malária falciparum pode evoluir para malignidade, levando à morte.
Durante seu ciclo de vida, os patógenos da malária passam pelo seguinte ciclo de desenvolvimento com mudança de hospedeiros:
- o desenvolvimento assexuado (esquizogonia) ocorre no corpo do hospedeiro intermediário - um humano;
- O desenvolvimento sexual (esporogonia) ocorre no corpo do hospedeiro final - o mosquito fêmea do gênero Anopheles.
Os esporozoítos entram no corpo humano através da picada de um mosquito da malária infectado. Após entrarem na corrente sanguínea, os esporozoítos penetram nos hepatócitos a partir dos vasos sinusoidais do fígado em 15 a 45 minutos e iniciam o ciclo exoeritrocítico (esquizogonia tecidual). A seletividade e a velocidade da invasão devem-se à presença de receptores específicos nas membranas dos hepatócitos. Os parasitas aumentam de tamanho, dividem-se repetidamente e formam muitas pequenas formações mononucleares - merozoítos. A duração mínima do ciclo exoeritrocítico é de 5 a 7 dias para P. falciparum, 6 a 8 dias para P. vivax, 9 dias para P. ovale e 14 a 16 dias para P. malariae. Em seguida, os merozoítos deixam os hepatócitos para a corrente sanguínea e penetram nos eritrócitos, onde ocorre a esquizogonia eritrocitária. A malária de três dias e a malária oval são caracterizadas por um tipo especial de desenvolvimento exoeritrocítico: todos os parasitas, ou alguns deles, são capazes de permanecer nos hepatócitos por um longo período (7 a 14 meses ou mais) em estado "dormente" (hipnozoítos), e somente após esse período começam a se transformar em merozoítos capazes de infectar eritrócitos. Isso determina a possibilidade de incubação prolongada e a ocorrência de recidivas remotas de até 3 anos.
A esquizogonia eritrocitária é acompanhada pelo desenvolvimento cíclico e pela divisão múltipla dos parasitas, com os plasmódios da malária passando pelos seguintes estágios: trofozoíto jovem (apresenta formato de anel); trofozoíto em desenvolvimento; trofozoíto maduro (apresenta núcleo grande); esquizonte em desenvolvimento; esquizonte maduro. Após a conclusão do processo de esquizogonia, o eritrócito é destruído. Os merozoítos livres penetram ativamente nos novos eritrócitos, mas a maioria deles morre devido aos efeitos dos mecanismos imunológicos protetores do hospedeiro. A duração da esquizogonia eritrocitária é de 48 horas em P. vivax, P. ovale, P. falciparum e 72 horas em P. malariae. Durante o ciclo eritrocitário, alguns merozoítos se transformam em formas sexuadas — femininas (macrogametócitos) ou masculinas (microgametócitos).
Os gametócitos entram no corpo do mosquito transmissor quando este se alimenta do sangue de um paciente com malária ou de um portador do parasita, contendo gametócitos maduros. No estômago do mosquito, após 9 a 12 minutos, o gametócito masculino ejeta oito finos flagelos móveis. Flagelos livres (microgametas) penetram na célula feminina (macrogameta); após a fusão dos núcleos, forma-se um zigoto - uma célula fertilizada e redonda. Em seguida, desenvolvem-se sucessivamente oocinetos, oocistos com esporozoítos, cuja maturação ocorre nas glândulas salivares do mosquito. Em uma temperatura ambiente ideal (25 °C), a esporogonia dura 10 dias em P. vivax, 12 dias em P. falciparum, 16 dias em P. malariae e P. ovale; em temperaturas do ar abaixo de 15 °C, os esporozoítos não se desenvolvem.
Patogênese
Todos os sintomas da malária são causados por esquizogonia eritrocítica – o crescimento e a reprodução de formas eritrocíticas assexuadas do parasita no sangue. A esquizogonia tecidual não se manifesta clinicamente.
Um ataque de malária está associado à conclusão da esquizogonia eritrocítica, à desintegração em massa de eritrócitos e à entrada no sangue de um grande número de merozoítos, produtos metabólicos de parasitas com propriedades pirogênicas e tóxicas que provocam o desenvolvimento de uma reação febril. Devido à natureza cíclica da esquizogonia eritrocítica, os ataques febris repetem-se a cada 48 horas na malária de três dias, oval e tropical, e a cada 72 horas na malária de quatro dias. Quando uma pessoa é infectada, uma população heterogênea de parasitas da malária entra no corpo, e a esquizogonia no período inicial ocorre de forma assíncrona, devido à qual o tipo de febre pode ser irregular. À medida que as reações imunológicas se desenvolvem, a capacidade de parasitar nos eritrócitos é preservada em uma geração principal de plasmódios, o que determina o ritmo febril característico desta espécie. Somente na malária tropical podem existir várias (2-3) gerações principais de plasmódios, por isso a febre é frequentemente irregular.
A anemia, característica da malária, é consequência da destruição dos glóbulos vermelhos por parasitas neles presentes. Sabe-se que P. vivax e P. ovale penetram principalmente nos glóbulos vermelhos jovens, enquanto P. malariae penetra nos maduros. P. falciparum infecta glóbulos vermelhos com diferentes graus de maturidade, o que contribui para danos mais significativos e hemólise; portanto, na malária tropical, a hemólise desempenha um papel fundamental na gênese da anemia. Fatores adicionais na hemólise dos glóbulos vermelhos também são mecanismos autoimunes que danificam os glóbulos vermelhos não infectados. A hiperplasia dos elementos reticuloendoteliais do baço, que se desenvolve na malária, inibe a hematopoiese, o que aumenta a anemia e a trombocitopenia.
O aumento do fígado e do baço é inicialmente causado pela congestão dos órgãos, mas logo ocorre hiperplasia linfoide e reticuloendotelial. Como resultado da hemólise dos eritrócitos, bem como da lesão dos hepatócitos, desenvolve-se icterícia. A diminuição da absorção de carboidratos e a inibição da gliconeogênese no fígado causam hipoglicemia. A ativação da glicólise anaeróbica leva ao acúmulo de lactato no sangue, no líquido cefalorraquidiano e à ocorrência de acidose láctica, uma das causas da malária tropical grave.
Na malária tropical, as propriedades dos eritrócitos se alteram, o que resulta na interrupção da microcirculação (citoadesão, sequestro, formação de rosetas). A citoadesão é a adesão de eritrócitos infectados às células endoteliais, causando o sequestro nos capilares e vênulas pós-capilares. O papel principal na citoadesão é atribuído a proteínas ligantes específicas (sua expressão na superfície dos eritrócitos é induzida pelo parasita) e a receptores localizados na superfície externa das células endoteliais. A oclusão dos vasos sanguíneos causa isquemia dos órgãos afetados. Protuberâncias (saliências) aparecem nas membranas dos eritrócitos, que entram em contato com protuberâncias em forma de pseudópodes formadas nas células endoteliais. Algumas variedades de P. falciparum fazem com que eritrócitos saudáveis adiram aos infectados, resultando na formação de "rosetas". Os glóbulos vermelhos tornam-se rígidos, o que piora as propriedades reológicas do sangue e agrava o distúrbio da microcirculação. Um importante fator prejudicial é a hipóxia causada pela função insuficiente de transporte de oxigênio dos glóbulos vermelhos infectados. O tecido cerebral é o menos resistente à hipóxia, o que contribui para o desenvolvimento da malária cerebral. Distúrbios no sistema de coagulação sanguínea ocorrem: na malária tropical grave, sinais de síndrome DIC, trombocitopenia e hipofibrinogenemia são observados. Um certo papel na patogênese da malária tropical é dado à reação inflamatória inespecífica generalizada. O dano vascular é causado principalmente pela ação de mediadores inflamatórios. Os mais ativos são os produtos de peroxidação lipídica e as proteases secretadas pelos granulócitos. Na patogênese da malária grave, considerável atenção é dada às citocinas, em particular TNF e IL-2 (IL-6). As alterações mais características da malária tropical grave ocorrem no cérebro, onde se observam edema, inchaço da massa encefálica e crescimentos perivasculares e periganglionares da neuróglia (granulomas de Durk). Os capilares são bloqueados por eritrócitos e parasitas invadidos; observa-se extensa hemostasia. Desenvolve-se edema perivascular com hemorragias e necrose focal. Com base no quadro patológico, pode-se concluir que, em casos de coma malárico, desenvolve-se meningoencefalite específica.
A infecção por malária pode interromper a resposta imune do hospedeiro, o que desencadeia uma cascata de reações imunopatológicas. A fixação de imunoglobulinas e complemento nas membranas basais glomerulares causa nefropatia aguda. A síndrome nefrótica, que se desenvolve em pacientes com malária de quatro dias, é classificada como uma glomerulopatia por imunocomplexos.
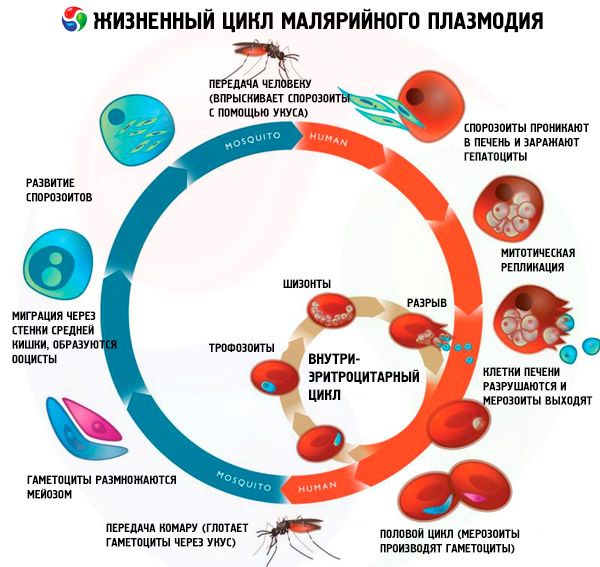
Ciclo de vida de todos os patógenos da malária
O ciclo de vida de todos os patógenos da malária inclui dois hospedeiros: humanos (esquizogonia - ciclo de desenvolvimento assexuado) e mosquitos do gênero Anopheles (esporogonia - ciclo de desenvolvimento sexual).
Tradicionalmente, distinguem-se três estágios no ciclo da esquizogonia de todas as espécies de parasitas da malária: esquizogonia exoeritrocítica (EESh), esquizogonia eritrocítica (ESH) e gametocitogonia. Além disso, distingue-se um estágio distinto nos ciclos de vida de Pl. vivax e Pl. ovale – a hibernação – devido à possível introdução de um grupo morfologicamente heterogêneo de esporozoítos (taquisporozoítos e bradisporozoítos ou apenas bradisporozoítos) no corpo humano durante uma picada de mosquito. Nesses casos, os bradisporozoítos (hipnozoítos) são preservados nos hepatócitos por um longo período em estado inativo até o início da EES.
 [ 19 ], [ 20 ], [ 21 ], [ 22 ]
[ 19 ], [ 20 ], [ 21 ], [ 22 ]
Esquizogonia exoeritrocítica
Os esporozoítos introduzidos no corpo humano pela saliva do mosquito entram muito rapidamente (em 15 a 30 minutos) no fígado com a corrente sanguínea, onde penetram ativamente nos hepatócitos sem danificá-los. Os esporozoítos de Pl. falciparum, Pl. malariae e os taquisporozoítos de Pl. vivax e Pl. ovale iniciam imediatamente a EES com a formação de um grande número de merozoítos exoeritrocíticos (até 40.000 a partir de um esporozoíto na malária falciparum). Os hepatócitos são destruídos e os merozoítos entram novamente na corrente sanguínea com subsequente penetração rápida (em 15 a 30 minutos) nos eritrócitos. A duração da EES para a malária falciparum é geralmente de 6 dias, para a malária vivax - 8 dias, para a malária ovofe - 9 dias, para a malária malariae - 15 dias.
 [ 23 ], [ 24 ], [ 25 ], [ 26 ], [ 27 ], [ 28 ], [ 29 ]
[ 23 ], [ 24 ], [ 25 ], [ 26 ], [ 27 ], [ 28 ], [ 29 ]
Estágio dormente
Na malária vivax e ovale, os bradisporozoítos que penetraram nos hepatócitos transformam-se em formas inativas – hipnozoítos, que podem permanecer sem se dividir por vários meses ou até anos até a reativação subsequente (divisão e formação de merozoítos). Assim, os hipnozoítos estão associados a uma longa incubação (até 3 a 10 meses ou mais) e ao desenvolvimento de recidivas exoeritrocíticas remotas, características apenas dessas formas de malária.
Esquizogonia eritrocitária
Após a introdução dos merozoítos nos eritrócitos, os parasitas da malária passam repetidamente (ciclicamente) sequencialmente pelos estágios de: trofozoíto (célula mononuclear que se alimenta), esquizonte (célula multinuclear em divisão) e mórula (parasitas formados localizados dentro do eritrócito). Posteriormente, após a destruição dos eritrócitos, os merozoítos entram no plasma sanguíneo. O maior número de merozoítos-filhos é formado na malária tropical – até 40 em um eritrócito. O estágio ES dura um tempo estritamente definido: 48 horas para malária falciparum, malária vivax, malária ovale e 72 horas para malariae.
Características do ciclo da esquizogonia eritrocítica e os principais mecanismos patogênicos de desenvolvimento de formas graves e complicadas de malária falciparum:
- acúmulo (sequestro) de eritrócitos invadidos contendo trofozoítos adultos (do estágio de trofozoíto amebóide), esquizontes nos vasos de órgãos internos, principalmente o cérebro, bem como os rins, fígado, intestinos, medula óssea, placenta, etc.;
- a formação das chamadas rosetas, constituídas por eritrócitos invadidos e não infectados;
- desenvolvimento de distúrbios da microcirculação, hipóxia tecidual, acidose metabólica (acúmulo significativo de ácido láctico);
- ativação do MFS (principalmente resposta imune Th-1) com aumento da síntese do fator de necrose tumoral-a, interferon-y, interleucina-1 e outras citocinas que danificam o endotélio vascular e causam adesão de eritrócitos ao endotélio dos vasos sanguíneos.
Nos últimos anos, o papel especial do aumento da síntese de óxido nítrico (NO) pelas células endoteliais vasculares cerebrais no desenvolvimento da forma cerebral da malária falciparum tem sido considerado.
Um importante mecanismo fisiopatológico no desenvolvimento de formas graves de malária por falciparum, em comparação com outras formas de malária, é a hipoglicemia, que agrava distúrbios microcirculatórios e metabólicos (acidose metabólica) em pacientes, especialmente em crianças e gestantes. Três fatores principais são distinguidos no desenvolvimento de hipoglicemia na malária por falciparum: diminuição da glicogênese hepática, utilização de glicose por parasitas e estimulação da secreção de insulina. Ao mesmo tempo, a hipoglicemia pode ser consequência da hiperinsulinemia que se desenvolve após a administração de quinina para interromper os ataques de malária por falciparum.
Como consequência da persistência prolongada do parasita (sem terapia adequada) na malária-malária, pode desenvolver-se a síndrome nefrótica, resultante de um mecanismo imunológico (deposição de complexos imunes contendo antígenos do parasita na membrana basal dos glomérulos renais).
Deve-se notar que as principais manifestações clínicas de todas as formas de malária (intoxicação, aumento do fígado e baço, anemia) estão associadas ao estágio de esquizogonia eritrocitária (reprodução assexuada repetida de parasitas em eritrócitos), e quanto maior o conteúdo de parasitas em 1 μl de sangue de um paciente, determinado por microscopia de esfregaço sanguíneo espesso, mais grave a malária geralmente é. Portanto, no diagnóstico laboratorial da malária, é importante não apenas estabelecer o tipo de plasmódio da malária, mas também determinar o nível de parasitemia. De acordo com o nível máximo de parasitemia, as formas de malária são distribuídas em ordem decrescente: malária falciparum (até 100 mil em μl ou mais), malária vivax (até 20 mil em μl, menos frequentemente mais), malária ovale e malária malariae (até 10-15 mil em μl). Na malária falciparum, que ocorre com alto nível de parasitemia (100 mil por μl e superior), o risco de desenvolver complicações graves e fatais aumenta significativamente, o que determina as táticas de terapia antimalárica intensiva (parenteral).
A ocorrência de paroxismos febris na malária é causada pela hemólise dos eritrócitos, liberação de merozoítos no plasma, destruição de alguns deles (a outra parte dos merozoítos é novamente introduzida nos eritrócitos), ativação do MFS e aumento da síntese de interleucina-1, -6, fator de necrose tumoral a e outros pirogênios endógenos (citocinas inflamatórias) que afetam o centro de termorregulação do hipotálamo.
Na presença de uma geração de plasmódios no sangue, ocorrem paroxismos regularmente alternados desde os primeiros dias da doença. Frequentemente, na malária falciparum e na malária vivax (em regiões hiperendêmicas com transmissão intensiva de malária), indivíduos não imunes apresentam uma febre inicial (inicial) associada ao desenvolvimento de várias gerações de patógenos nos eritrócitos dos pacientes simultaneamente, com diferentes tempos para o final do ciclo de desenvolvimento, o que leva à sobreposição de crises, suavizando o período de apirexia e distorcendo o paroxismo típico.
À medida que a doença progride, os fatores de defesa específicos e não específicos aumentam (até o final da 1ª-2ª semana), algumas gerações morrem e uma (duas) gerações líderes de parasitas permanecem com o desenvolvimento de paroxismos típicos em dias alternados (ou todos os dias).
O aumento do fígado e do baço em todas as formas de malária está associado ao significativo enchimento sanguíneo, edema e hiperplasia da articulação metastática.
A malária, via de regra, sempre leva à anemia hemolítica hipocrômica, em cuja patogênese vários fatores são importantes:
- hemólise intravascular de eritrócitos infectados;
- fagocitose de eritrócitos infectados e não infectados por células reticuloendoteliais do baço;
- sequestro (acúmulo) de eritrócitos contendo parasitas maduros na medula óssea, supressão da hematopoiese;
- mecanismo imunológico (destruição de eritrócitos não afetados como resultado da adsorção de complexos imunes contendo a fração C-3 do complemento na membrana do eritrócito).
O estágio de gametocitogonia é uma espécie de ramificação do estágio ES. Alguns dos merozoítos (um processo geneticamente determinado), em vez de repetir o ciclo de desenvolvimento assexuado após serem introduzidos no eritrócito, transformam-se em formas sexuadas — gametócitos (masculinos e femininos).
Características do estágio gametocitogonial na malária falciparum:
- os gametócitos aparecem no sangue periférico não antes de 10-12 dias da doença;
- Os gametócitos, acumulados durante o curso da doença, podem circular na corrente sanguínea por um longo período (até 4 a 6 semanas ou mais).
Em outras formas de malária (vivax, ovale, malariae), os gametócitos podem ser detectados no sangue periférico desde os primeiros dias da doença e morrem rapidamente (dentro de algumas horas ou dias).
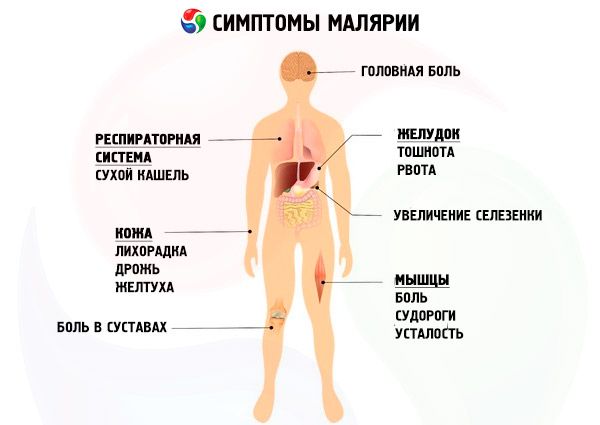
Sintomas malária
Levando em consideração as características das espécies de parasitas da malária e os sintomas correspondentes da malária, distinguem-se quatro formas da doença: malária de três dias (malária vivax, malária tertiana), malária de quatro dias (malária quartana), malária tropical (malária falciparum, malária tropica), malária oval de três dias (malária ovale).
O curso da malária primária inclui o período inicial da doença, o pico da doença e a recuperação. Sem tratamento ou com terapia etiotrópica inadequada, a malária entra em um período de recaída. Existem recaídas exoeritrocíticas e eritrocíticas, de acordo com o tempo de desenvolvimento - precoces e tardias. Recaídas eritrocíticas são observadas na infecção por todos os tipos de plasmódios. As recaídas precoces ocorrem dentro de 2 meses após os ataques primários; as recaídas que se desenvolvem posteriormente são consideradas tardias. Sem tratamento ou com tratamento inadequado da malária de três dias e ovale, ocorre uma "calmaria" com duração de 6 a 11 meses, com o desaparecimento dos parasitas do sangue e o bem-estar clínico. Em seguida, ocorrem as recaídas tardias (causadas pela ativação de hipnozoítos no fígado), novamente substituídas por um período latente sem tratamento, após o qual a doença reaparece.
P. falciparum vive no corpo humano (sem tratamento) por até 1,5 anos, P. vivax e P. ovale - até 3 anos, P. malariae - por muitos anos, às vezes por toda a vida.
O que está incomodando você?
Formulários
De acordo com as recomendações da OMS, a malária é dividida em não complicada, grave e complicada. As formas malignas da malária e suas complicações são características principalmente da infecção por P. falciparum. A doença causada por P. vivax, P. ovale e P. malariae, em geral, tem um curso benigno.
Malária de três dias
O período de incubação da malária de três dias varia de 10 a 21 dias a 6 a 14 meses. Os sintomas prodrômicos da malária antes do ataque primário são raramente observados, mas frequentemente precedem as recidivas e se manifestam por uma sensação de mal-estar geral, fraqueza, fadiga, dor na região lombar e nos membros, leve aumento da temperatura corporal, perda de apetite e dor de cabeça. A duração média do período prodrômico é de 1 a 5 dias.
Inicialmente, a curva de temperatura é irregular (febre inicial), o que está associado à liberação assíncrona de várias gerações de P. vivax no sangue. Posteriormente, os ataques típicos de malária começam com febre intermitente de três dias, indicando a formação da principal geração de parasitas no sangue. Em um ataque febril de malária, três fases são clinicamente claramente expressas, imediatamente sucessivas: a fase de calafrios, calor e suor. Um ataque de malária começa com calafrios, cuja intensidade pode variar de tremores leves a calafrios intensos. Nesse momento, o paciente vai para a cama e tenta, sem sucesso, se aquecer, mas os calafrios aumentam. A pele fica seca, áspera ou "arrepiada" ao toque, fria, as extremidades e as mucosas visíveis ficam cianóticas. Os seguintes sintomas de malária são observados: dor de cabeça intensa, às vezes vômitos, dor nas articulações e na região lombar. A fase de calafrios dura de alguns minutos a 1 a 2 horas e é substituída pela fase febril. O paciente tira a roupa e a roupa íntima, mas isso não lhe traz alívio. A temperatura corporal atinge 40-41 °C, a pele fica seca e quente, o rosto fica vermelho. Dor de cabeça, dor na região lombar e nas articulações se intensificam, delírio e confusão são possíveis. A fase febril dura de uma a várias horas e é substituída por um período de suor. A temperatura cai criticamente, a sudorese é frequentemente abundante, então o paciente tem que trocar de roupa íntima repetidamente. Enfraquecido pelo ataque, ele logo adormece. A duração do ataque é de 6 a 10 horas. O início dos ataques da doença nas horas da manhã e da tarde é considerado típico. Após o ataque, inicia-se um período de apirexia, com duração de cerca de 40 horas. Após 2 a 3 ataques de temperatura, o fígado e o baço estão claramente aumentados. Alterações no sangue: anemia, desenvolvendo-se gradualmente a partir da segunda semana da doença, leucopenia, neutropenia com desvio de bastonetes para a esquerda, linfocitose relativa, aneosinofilia e aumento da VHS.
No curso natural da doença sem tratamento etiotrópico, após 12 a 14 crises (4 a 6 semanas), a intensidade da febre diminui, as crises diminuem gradualmente e o tamanho do fígado e do baço diminui. No entanto, após 2 semanas a 2 meses, ocorrem recidivas precoces, caracterizadas por uma curva de temperatura sincronizada, aumento do fígado e do baço e anemia. Posteriormente, com o aumento da imunidade, os parasitas desaparecem do sangue e inicia-se um período latente. Se o tratamento com medicamentos histoesquizotrópicos não for realizado nesse período, após 6 a 8 meses (e às vezes após 1 a 3 anos), ocorre a ativação das formas teciduais "latentes" dos parasitas e desenvolvem-se recidivas remotas. Elas são caracterizadas por um início agudo, um curso mais brando, um aumento precoce do baço, um pequeno número de crises (até 7 a 8), menor intensidade e duração da parasitemia e presença de gametócitos no sangue.
Malária ovale
Em muitas características clínicas e patogênicas, a malária oval é semelhante à malária vivax de três dias. O período de incubação da malária oval é de 11 a 16 dias. Na malária oval, o patógeno tende à latência primária. O período de incubação pode durar de 2 meses a 2 anos ou mais. Os sintomas da malária incluem febre intermitente de três dias, sendo menos comum a febre diária. Os ataques febris ocorrem frequentemente à noite, em vez de na primeira metade do dia, como é típico de outras formas de malária. A malária oval é caracterizada principalmente por um curso leve, com um pequeno número de paroxismos que ocorrem sem calafrios pronunciados e com uma temperatura mais baixa no pico dos ataques. É característico que os paroxismos durante o ataque primário muitas vezes cessem espontaneamente. Isso se explica pela rápida formação de imunidade estável. Se o tratamento com medicamentos histoesquizotrópicos não for realizado, são possíveis de 1 a 3 recidivas, com um intervalo entre recidivas de 17 dias a 7 meses.
Quartã
Geralmente, a malária evolui de forma benigna. O período de incubação é de 3 a 6 semanas. Os sintomas prodrômicos da malária são raros. O início da doença é agudo. Desde o primeiro ataque, estabelece-se febre intermitente, com crises a cada 2 dias. O paroxismo geralmente começa ao meio-dia e dura em média 13 horas. O período de calafrios é longo e intenso. O período de febre dura até 6 horas e é acompanhado por cefaleia, mialgia, artralgia, às vezes náuseas e vômitos. Às vezes, os pacientes ficam inquietos e delirantes. No período interictal, o estado dos pacientes é satisfatório. Anemia e hepatoesplenomegalia desenvolvem-se lentamente, não antes de 2 semanas após o início da doença. Sem tratamento, observam-se de 8 a 14 crises, mas o processo de esquizogonia eritrocitária em níveis baixos dura muitos anos. Na maioria das vezes, a infecção ocorre na forma de parasita sem ativação da esquizogonia eritrocitária, o que torna esses indivíduos doadores potencialmente perigosos. Em focos endêmicos, a malária de quatro dias causa síndrome nefrótica com prognóstico desfavorável em crianças.
Malária tropical
A forma mais grave de infecção por malária. O período de incubação é de 8 a 16 dias. Ao final dele, alguns indivíduos não imunes apresentam sintomas prodrômicos de malária, que duram de várias horas a 1 a 2 dias: mal-estar, fraqueza, fadiga, dores no corpo, mialgia e artralgia, e dor de cabeça. Na maioria dos pacientes, a malária tropical inicia-se de forma aguda, sem período prodrômico, com aumento da temperatura corporal para 38-39 °C. Se os ciclos de esquizogonia eritrocítica em várias gerações de P. falciparum em um organismo infectado não terminam simultaneamente, isso frequentemente se expressa clinicamente pela ausência de uma periodicidade cíclica de crises febris. As crises, que ocorrem com uma mudança alternada de fases, começam com calafrios que duram de 30 minutos a 1 hora. Durante esse período, a pele fica pálida ao exame, fria ao toque, frequentemente com uma aspereza semelhante a "arrepios". Os calafrios são acompanhados por um aumento da temperatura corporal para 38-39 °C. Com a cessação dos calafrios, inicia-se a segunda fase do paroxismo: a febre. Os pacientes experimentam uma leve sensação de calor, às vezes uma sensação de calor intenso. A pele fica quente ao toque e o rosto fica hiperêmico. A duração dessa fase é de cerca de 12 horas, sendo substituída por sudorese leve. A temperatura corporal cai para valores normais e abaixo do normal e, após 1 a 2 horas, volta a subir. Em alguns casos, o início da malária tropical é acompanhado por náuseas, vômitos e diarreia. Às vezes, são registrados sintomas catarrais da malária do trato respiratório superior: tosse, coriza e dor de garganta. Em um estágio posterior, observam-se erupções herpéticas nos lábios e nas asas do nariz. Na fase aguda, os pacientes notam hiperemia da conjuntiva; em casos graves, pode ser acompanhada por petéquias ou hemorragias subconjuntivais maiores.
Durante o pico da malária tropical, os calafrios são menos pronunciados do que nos primeiros dias da doença, durando de 15 a 30 minutos. A febre persiste por vários dias e raramente são registrados períodos de apirexia. Em um curso leve da doença, a temperatura corporal atinge o pico de 38,5 °C, a duração da febre é de 3 a 4 dias; com um grau moderado de gravidade, 39,5 °C e 6 a 7 dias, respectivamente. O curso grave da doença é caracterizado por um aumento da temperatura corporal para 40 °C ou mais, e sua duração é de oito dias ou mais. A duração dos paroxismos individuais (e, na verdade, a estratificação de vários) na malária tropical chega a 30 a 40 horas. Predomina o tipo irregular de curva de temperatura, sendo menos frequentemente observados os tipos remitente, ocasionalmente intermitente e constante.
O aumento do fígado é geralmente determinado no 3º dia da doença, o aumento do baço - também a partir do 3º dia, mas geralmente é registrado apenas por percussão; a palpação clara só se torna possível no 5º-6º dia. Durante o exame ultrassonográfico dos órgãos abdominais, o aumento do fígado e do baço é determinado já no 2º-3º dia após o aparecimento das manifestações clínicas da malária tropical. Distúrbios do metabolismo pigmentar são observados apenas em pacientes com malária tropical grave e, menos frequentemente, moderada. Um aumento de mais de três vezes na atividade sérica das aminotransferases é considerado um indicador de um prognóstico desfavorável. Os distúrbios metabólicos na malária tropical incluem alterações no sistema de hemostasia e hipoglicemia. Os distúrbios cardiovasculares são de natureza funcional e se expressam por taquicardia, sons cardíacos abafados e hipotensão. Ocasionalmente, um sopro sistólico transitório é ouvido no ápice do coração. Nas formas graves da doença, observam-se alterações no ECG na forma de deformação da parte terminal do complexo ventricular: achatamento e configuração inversa da onda T, rebaixamento do segmento ST. Ao mesmo tempo, a voltagem das ondas R nas derivações padrão diminui. Em pacientes com a forma cerebral, as alterações na onda P são do tipo P-pulmonale.
Na malária tropical, são frequentemente observados distúrbios do SNC associados a febre alta e intoxicação: dor de cabeça, vômitos, meningismo, convulsões, sonolência, às vezes síndrome semelhante ao delírio, mas a consciência do paciente é preservada.
Os sinais característicos da infecção por malária moderada e grave são anemia hemolítica e leucopenia, eosinofilia e neutropenia, e linfocitose relativa é observada na fórmula leucocitária. Nas formas graves da doença, é possível a leucocitose neutrofílica; a VHS está constante e significativamente elevada. A trombocitopenia é um sinal típico de todos os tipos de malária. Assim como em outras doenças infecciosas, os pacientes apresentam proteinúria transitória.
A malária tropical recorrente é causada por tratamento etiotrópico inadequado ou pela resistência do P. falciparum aos agentes quimioterápicos utilizados. O curso natural da malária tropical com desfecho favorável não dura mais de 2 semanas. Na ausência de terapia etiotrópica, as recidivas ocorrem após 7 a 10 dias.
A gravidez é um fator de risco geralmente reconhecido para a malária tropical. Isso se deve à maior incidência de gravidez, à tendência a formas clínicas graves, ao risco à saúde e à vida da criança e ao arsenal terapêutico limitado. A malária tropical em crianças menores de cinco anos deve ser considerada uma doença potencialmente fatal. Em crianças de faixas etárias mais jovens (até 3-4 anos), especialmente em bebês, a malária apresenta um quadro clínico único: não apresenta o sintoma clínico mais marcante - o paroxismo da malária. Ao mesmo tempo, sintomas de malária como convulsões, vômitos, diarreia e dor abdominal são observados, com uma rápida deterioração progressiva do estado da criança. O aparecimento de convulsões e outros sintomas cerebrais não significa necessariamente o desenvolvimento de malária cerebral - este é frequentemente um dos sintomas de neurotoxicose. A parasitemia em crianças pequenas costuma ser alta: o P. falciparum pode afetar até 20% dos glóbulos vermelhos. A doença pode rapidamente se tornar maligna e resultar na morte da criança.
Complicações e consequências
Registrado em todos os estágios da malária tropical. Sintomas de malária com prognóstico desfavorável, indicando a possibilidade de desenvolvimento de uma forma maligna da doença. - febre diária, ausência de apirexia entre as crises, cefaleia intensa, convulsões generalizadas recorrentes mais de duas vezes em 24 horas, rigidez descerebrada, choque hemodinâmico (pressão arterial sistólica abaixo de 70 mm Hg em um adulto e menos de 50 mm Hg em uma criança). Isso também é evidenciado por alta parasitemia (mais de 100 mil P. falciparum em 1 μl de sangue), detecção de diferentes estágios etários do parasita no sangue periférico, presença de gametócitos e aumento da leucocitose (mais de 12,0x10 9 /l). Hipoglicemia menor que 2,2 mmol/L, acidose metabólica descompensada, aumento de mais de três vezes na atividade das aminotransferases séricas, bem como diminuição do nível de glicose no líquido cefalorraquidiano e nível de lactato maior que 6 μmol/L também são prognósticos desfavoráveis.
Lesões graves do SNC na malária tropical são agrupadas sob o nome de "malária cerebral", cujo principal sintoma é o desenvolvimento de um estado comatoso. O coma malárico pode ser uma complicação da malária primária, recorrente e de repetição, mas é mais frequentemente observado na malária primária, principalmente em crianças, gestantes e pessoas jovens e de meia-idade.
A forma cerebral é a complicação mais comum da malária falciparum grave. Nas condições atuais, a forma cerebral se desenvolve em 10% de todos os casos de malária falciparum no mundo, e 60 a 80% de todos os desfechos fatais da doença estão associados a essa complicação. A forma cerebral pode se desenvolver desde os primeiros dias, mas é mais frequentemente registrada na segunda semana da doença devido à ausência de terapia específica ou inadequada. Um desfecho fatal pode ocorrer em 1 a 2 dias. No quadro clínico da malária cerebral, distinguem-se três períodos: atordoamento, estupor e coma verdadeiro.
O estágio de estupor é caracterizado pela letargia mental e física do paciente, com exaustão rápida. Ele se orienta no tempo e no espaço, mas reluta em estabelecer contato, responde a perguntas em monossílabos e se cansa rapidamente. Os reflexos tendinosos são preservados.
O estágio de sopor se manifesta por prostração profunda do paciente com raros lampejos de consciência. Ataxia, amnésia e convulsões, às vezes de natureza epileptiforme, são possíveis. Os reflexos corneanos estão preservados e as pupilas estão normais. Os reflexos tendinosos estão aumentados e ocorrem reflexos patológicos.
Em coma, o paciente está inconsciente e não responde a estímulos externos. Observam-se distúrbios de convergência, estrabismo divergente, movimentos flutuantes dos globos oculares com as pálpebras abertas (como se o paciente estivesse olhando para o teto), nistagmo horizontal e vertical, paralisia do sexto par de nervos cranianos; os reflexos tendinosos e abdominais estão ausentes, as funções vegetativas são gravemente prejudicadas. Sintomas meníngeos de malária e reflexos patológicos de Babinski, Rossolimo, etc. são expressos. Observa-se incontinência urinária e fecal. Uma punção lombar revela um aumento da pressão intracraniana sem distúrbios pronunciados na composição proteica e celular do líquido cefalorraquidiano. Um alto grau de parasitemia com vários estágios etários de P. falciparum é determinado em uma gota espessa e esfregaço sanguíneo de pacientes com malária em coma. Ao mesmo tempo, são conhecidos casos de desfechos fatais de malária cerebral com um nível muito baixo de parasitemia. A malária cerebral em crianças é frequentemente acompanhada de anemia. A anemia agrava a condição neurológica e somática da criança. Com tratamento eficaz, a consciência geralmente retorna repentinamente.
Na malária cerebral, as psicoses podem se desenvolver como consequência de alterações distróficas no parênquima cerebral. No período agudo, as psicoses ocorrem na forma de delírio, amência, crises epilépticas e estados maníacos. As psicoses pós-malária são caracterizadas por depressão, fraqueza mental, histeria, síndromes semelhantes à esquizofrenia e, em crianças, atraso temporário no desenvolvimento mental. Às vezes, observam-se consequências remotas da malária cerebral: hemiplegia, ataxia, sintomas focais dos nervos cranianos, distúrbios extrapiramidais, mono e polineurite.
Uma complicação comum de todas as formas de infecção por malária é a anemia hipocrômica. A anemia grave é diagnosticada quando o hematócrito cai para menos de 20% e o nível de hemoglobina é inferior a 50 g/l. O grau de anemia depende do tipo de parasita, bem como da intensidade e duração da infecção. A gravidade da malária em povos indígenas de países tropicais é frequentemente agravada pela deficiência de ferro e ácido fólico na dieta. Após os primeiros ataques de malária, pode ocorrer anemia, que é mais pronunciada na malária tropical do que em outras formas.
O choque tóxico infeccioso (ITS) com desenvolvimento de síndrome da coagulação intravascular disseminada (CID) é uma complicação característica da malária-falciforme, que ocorre com alta parasitemia. O desenvolvimento de insuficiência adrenal aguda é característico. O curso do choque tóxico infeccioso em climas quentes é acompanhado de hipovolemia.
O desenvolvimento de insuficiência renal aguda é geralmente observado no curso maligno e complicado da malária falciparum. O desenvolvimento de oligúria e anúria com aumento de creatinina e ureia no sangue é característico; a análise da urina revela proteinúria, cilindrúria, piúria e microhematúria pronunciadas.
A síndrome nefrótica é uma complicação característica da malária, caracterizada por um curso lento e progressivo, acompanhado de edema, hipertensão arterial, proteinúria e desenvolvimento de insuficiência renal.
A febre hemoglobinúrica é consequência de hemólise intravascular maciça, tanto com invasão intensa quanto como resultado do uso de alguns medicamentos antimaláricos (quinino, primaquina, sulfonamidas) em indivíduos com deficiência da enzima glicose-6-fosfato desidrogenase. Em sua forma grave, desenvolvem-se icterícia intensa, síndrome hemorrágica grave, anemia e anúria, acompanhadas de calafrios, febre (40 °C), dor na região lombar, vômitos repetidos de bile, mialgia e artralgia. A urina adquire uma cor marrom-escura, devido à presença de oxihemoglobina. O número de eritrócitos em casos graves é reduzido para 1x10 12 /l, e o nível de hemoglobina cai para 20-30 g /l. Há muito poucos parasitas no sangue com hemoglobinúria malárica ou eles não são detectados. Com a rápida retirada do medicamento antimalárico que causou hemólise dos glóbulos vermelhos, a condição do paciente melhora sem consequências graves. Em casos graves, devido ao desenvolvimento de insuficiência renal aguda, o prognóstico pode ser desfavorável. Nos últimos anos, tem-se considerado a natureza autoimune do desenvolvimento de hemólise aguda associada ao uso prolongado e frequente de medicamentos antimaláricos – quinina e primaquina. Observa-se febre alta (com parasitemia leve), urina escurecida, anemia, leucocitose, VHS acelerada são determinados no exame de sangue, e a insuficiência renal progride rapidamente, o que leva à morte na ausência de terapia adequada.
A álgide malárica é caracterizada por manifestações clínicas típicas do choque tóxico infeccioso: distúrbios hemodinâmicos e da microcirculação, distúrbios do sistema de hemostasia, falência múltipla de órgãos e hipotermia. Ao contrário da malária cerebral, a consciência é preservada, embora o coma possa se desenvolver posteriormente. A álgide pode se desenvolver em um contexto de edema pulmonar, acidose metabólica e desidratação grave. Observa-se um alto nível de parasitemia. O prognóstico depende em grande parte do tratamento oportuno e correto.
O edema pulmonar agudo em pacientes com malária tropical frequentemente leva à morte. O mecanismo dessa complicação grave ainda não foi totalmente compreendido. O edema pulmonar pode ser provocado pela reidratação excessiva, mas também pode se desenvolver em condições de pressão normal na circulação pulmonar. Atualmente, a maioria dos pesquisadores considera a insuficiência respiratória aguda na malária tropical como uma manifestação da síndrome do desconforto respiratório do adulto.
Uma complicação rara, porém grave, de qualquer forma clínica de malária, com ou sem esplenomegalia hiper-reativa, é a ruptura esplênica. A ruptura pode ser causada por torção do pedículo esplênico com estase sanguínea aguda e desenvolvimento de hematoma subcapsular.
Na malária tropical, são possíveis lesões da córnea do olho, irite, iridociclite, opacificação do corpo vítreo, neurite óptica, coriorretinite e hemorragias retinianas; há relatos de paralisia dos músculos oculares causada por lesões dos III, IV e VI pares de nervos cranianos e paralisia da acomodação.
Recaídas de malária
O nível de parasitemia durante uma recaída é geralmente menor do que durante os sintomas primários da malária. Devido ao aumento do limiar pirogênico durante o curso da infecção, as manifestações clínicas durante uma recaída geralmente ocorrem com parasitemia mais alta. As recaídas, em regra, prosseguem benignamente, com uma síndrome tóxica moderadamente expressa e uma alternância regular de paroxismos maláricos desde o início da recaída; o número de paroxismos é significativamente menor do que durante as manifestações primárias da doença. De acordo com o tempo de início, distinguem-se as recaídas precoces (desenvolvimento de manifestações clínicas durante os primeiros 2 meses após as manifestações primárias da malária) e tardias (após 2 meses). De acordo com a origem, as recaídas são divididas em eritrocíticas (todas as formas de malária) e exoeritrocíticas (apenas na malária vivax e ovale).
Diagnósticos malária
O diagnóstico da malária baseia-se em dados epidemiológicos (permanência em foco de malária, ausência ou insuficiência de quimioprofilaxia), no quadro clínico da doença (crises características) e é confirmado por exames laboratoriais.
O diagnóstico da malária deve levar em consideração:
- início agudo da doença, sintomas pronunciados de intoxicação, curso cíclico com ataques alternados de febre e períodos de apirexia, aumento do fígado e do baço, desenvolvimento de anemia hemolítica progressiva;
- dados de histórico epidemiológico (permanência em área de alto risco de malária, transfusão de sangue, dependência química);
Duração da malária, considerando o desenvolvimento de recidivas com uma única infecção e sem terapia etiotrópica adequada
Forma de malária |
Duração da infecção |
|
Normal |
Máximo |
|
Malária falciparum |
Até 1 ano |
Até 3 anos |
Malária-malária |
Até 2-3 anos |
Possível para a vida |
Malária-vivax e ovale |
Até 1,5-2 anos |
Até 4-5 anos |
- resultados de testes laboratoriais:
- resultados do hemograma: diminuição dos níveis de hemoglobina, leucopenia, linfomonocitose, aumento da VHS;
- resultados da microscopia de uma gota espessa de sangue (visualização de pelo menos 100 campos de visão em casos de baixa parasitemia): detecção de plasmódios e determinação do nível de parasitemia em 1 µl de sangue (100 campos de visão - 0,2 µl de sangue).
Isto é necessário:
- Selecionar o grau de intensidade da terapia antimalárica específica (com alto nível de parasitemia em pacientes com malária tropical, a administração parenteral de medicamentos é preferível).
- Para monitorar a eficácia de uma terapia específica.
O nível de parasitemia também pode ser avaliado pela contagem da porcentagem de eritrócitos afetados por 100 leucócitos em uma gota espessa de sangue (neste caso, para avaliar o número de parasitas em 1 μl, é necessário saber o número total de leucócitos e eritrócitos em 1 μl no paciente);
- Dados microscópicos de um esfregaço de sangue para determinar o tipo de plasmódio. A gota espessa e o esfregaço de sangue são corados pelo método de Romanovsky-Giemsa.
Devido ao acúmulo de eritrócitos invadidos contendo trofozoítos e esquizontes adultos nos vasos dos órgãos internos, ao examinar uma preparação de gota espessa na malária por falciparum leve, apenas trofozoítos jovens (juvenis) no estágio de anel são determinados nos eritrócitos. O aparecimento no sangue periférico de eritrócitos invadidos contendo estágios adultos de desenvolvimento do parasita (trofozoítos adultos ou ameboides, esquizontes) é um sinal laboratorial desfavorável, indicando um curso grave (complicado) da malária por falciparum.
Graus de parasitemia na malária
Graus de parasitemia |
Designação convencional |
Número de parasitas nos campos visuais |
O número de parasitas em 1 µl de sangue |
4 |
+ |
1-20 em 100 campos |
5-50 |
III |
++ |
10-100 em 100 campos |
50-500 |
II |
+ + + |
1-10 em 1 campo |
500-5000 |
EU |
+ + + + |
Mais de 10 em 1 campo |
Mais de 5000 |
Em indivíduos que tiveram primeiro contato (não imunes) com essa infecção, crianças pequenas, os primeiros ataques podem ocorrer com parasitemia muito baixa, às vezes não detectável pela microscopia; isso requer um novo exame de sangue (gota espessa) após 6 a 12 horas, mas não depois de 24 horas.
O diagnóstico laboratorial da malária envolve o exame microscópico de amostras de sangue (métodos de gota espessa e esfregaço fino) coradas de acordo com Romanovsky-Giemsa.
Os seguintes pacientes estão sujeitos a exame para malária: pacientes febris com diagnóstico não especificado por 3 dias durante a estação epidêmica e 5 dias durante o resto do ano; pacientes com aumentos periódicos contínuos na temperatura corporal, apesar do tratamento de acordo com o diagnóstico estabelecido; receptores de sangue com aumento da temperatura corporal nos últimos 3 meses após a transfusão; pessoas que vivem em um foco ativo, com qualquer aumento na temperatura corporal. Deve-se levar em consideração que, durante os primeiros ataques de malária, o número de parasitas no sangue periférico é pequeno, portanto, o exame mais completo é necessário. A malária com baixa parasitemia também ocorre em pessoas que tomaram medicamentos antimaláricos para fins profiláticos (terapia supressora) ou medicamentos (tetraciclina, sulfonamidas) que têm um efeito supressor sobre os plasmódios da malária antes da doença. Recomenda-se que a coleta de sangue para exame seja realizada durante a febre e a apirexia. Para detectar parasitas, uma gota espessa é examinada, pois o volume de sangue nela é 30 a 40 vezes maior do que em um esfregaço fino. Em caso de alta parasitemia, o patógeno da malária é detectado mesmo ao examinar um esfregaço fino. As características morfológicas e as propriedades tintoriais (coloração) de diferentes estágios etários de formas assexuadas em eritrócitos são claramente distinguíveis em um esfregaço fino. É necessário determinar o tipo de parasita: isso é especialmente importante para P. falciparum. Na malária tropical não complicada, P. falciparum é observado no sangue periférico apenas no estágio de trofozoítos jovens em forma de anel. Em caso de infecção primária, estágios mais maduros do parasita são detectados no sangue periférico quando a doença tem um curso maligno grave. A parasitemia aumenta mais rapidamente do que com a infecção por outros tipos de patógenos. Os gametócitos de P. falciparum amadurecem lentamente, mas vivem por muito tempo (até 6 semanas), enquanto os gametócitos de outras espécies morrem várias horas após sua maturação. Os gametócitos detectados na malária tropical ajudam a determinar o período da doença: no período inicial (com curso descomplicado), apenas trofozoítos em forma de anel são detectados; durante o período de pico, anéis e gametócitos são detectados (com infecção primária na ausência de tratamento, isso indica que a malária dura pelo menos 10 a 12 dias); no período de recuperação, apenas gametócitos são encontrados. Durante o tratamento, o nível de parasitemia no sangue periférico é determinado dinamicamente. Um dia após o início do tratamento etiotrópico, deve diminuir em 25% ou mais e, no terceiro dia, não deve exceder 25% do original. A presença de parasitas na preparação sanguínea no quarto dia após o início do tratamento, sujeita a todas as condições para o sucesso do tratamento, é um sinal de resistência do patógeno ao medicamento utilizado.
Nos últimos anos, testes rápidos (métodos imunocromatográficos) baseados na detecção da proteína específica HRP-2a e da enzima pLDH de P. falciparum têm sido utilizados em focos endêmicos para obter rapidamente uma resposta preliminar. Testes de um dos conhecidos testes rápidos KAT-PF (KAT MEDICAL, África do Sul) demonstraram alta eficiência e especificidade em relação a P. falciparum. A comparação dos resultados do teste rápido, microscopia e PCR mostrou que sua eficiência diagnóstica atinge 95-98%. O uso de testes rápidos permite que você descubra o resultado em apenas 10 minutos. A equipe de laboratório pode dominar a reação em 1-2 horas. Os métodos rápidos permitem que pessoas que vivem ou viajam em regiões endêmicas realizem o autodiagnóstico; eles podem ser realizados em campo. Na Rússia, o diagnóstico rápido da malária está atualmente limitado a estudos clínicos individuais.
Em condições modernas, especialmente em estudos de massa, o método de PCR baseado na detecção do DNA do parasita da malária é de particular importância. O método pode ser usado para determinar a presença de parasitemia baixa e infecção mista com diferentes tipos de plasmódios, bem como para diferenciar a recidiva da malária falciparum resistente a medicamentos da reinfecção por P. falciparum. Atualmente, é usado principalmente em estudos epidemiológicos.
Quais testes são necessários?
Diagnóstico diferencial
A busca diagnóstica diferencial para malária é realizada dependendo da gravidade das manifestações clínicas da doença e de sua duração. Primeiramente, a malária é diferenciada de doenças que cursam com febre prolongada, aumento do fígado e do baço e possível desenvolvimento de anemia: febre tifoide e febre paratifoide, brucelose, leptospirose, sepse e linfogranulomatose. Nos primeiros 5 dias após o início da doença, um diagnóstico errôneo comum para malária em regiões não endêmicas é a gripe (ou outras infecções virais respiratórias agudas).
Em países tropicais da América do Sul, África, Sudeste Asiático e Índia, é realizado o diagnóstico diferencial da malária com febres virais hemorrágicas (febre amarela, dengue, etc.).
Na forma cerebral da malária falciparum, o diagnóstico diferencial da malária é realizado com encefalopatia (coma) que se desenvolve com diabetes mellitus descompensado, insuficiência hepática e renal, bem como edema e inchaço do cérebro com meningite ou meningoencefalite de etiologia bacteriana ou viral.
Quem contactar?
Tratamento malária
O tratamento da malária inclui interromper os ataques agudos da doença, prevenir recaídas e a transmissão de gametas, e restaurar as funções corporais prejudicadas.
Os medicamentos antimaláricos são divididos nos seguintes grupos, dependendo do seu efeito em um estágio específico do desenvolvimento do parasita: agentes hematoesquizotrópicos, eficazes contra estágios eritrocitários assexuados dos plasmódios; agentes histoesquizotrópicos, eficazes contra estágios teciduais assexuados dos plasmódios; medicamentos gamotrópicos, que causam a morte de gametócitos no sangue do paciente ou interrompem a maturação dos gamemontes e a formação de esporozoítos no corpo do mosquito.
Tratamento etiotrópico
O tratamento etiotrópico da malária em pacientes com malária deve ser prescrito imediatamente após o estabelecimento do diagnóstico clínico e epidemiológico e a coleta de sangue para exame parasitológico.
Os medicamentos atualmente utilizados pertencem a seis grupos de compostos químicos: 4-aminoquinolinas (cloroquina - delagil, fosfato de cloroquina, nivaquina), quinolinametanol (quinina - dicloridrato de quinina, sulfato de quinina, quinimax, mefloquina), fenantrenometanol (halfan, halofantrina), derivados de artemisinina (artesunato, arteméter, arteéter), antimetabólitos (proguanil), 8-aminoquinolinas (primaquina, tafenoquina). Além disso, são utilizados medicamentos antimaláricos combinados: savarina (cloroquina + proguanil), malarona (atovaquona + proguanil), coartem ou riamet (arteméter + lumefantrina).
Se P. vivax, P. ovale ou P. malariae forem detectados no paciente, medicamentos do grupo das 4-aminoquinolinas são usados, mais frequentemente cloroquina (delagyl). O tratamento da malária é o seguinte: nos dois primeiros dias, o medicamento é usado na dose diária de 10 mg/kg da base (quatro comprimidos de delagyl por vez), no terceiro dia - 5 mg/kg (dois comprimidos de delagyl) uma vez. Há relatos isolados de resistência de cepas de P. vivax à cloroquina na Birmânia, Indonésia, Papua Nova Guiné e Vanuatu. Nesses casos, o tratamento deve ser realizado com mefloquina ou quinina, de acordo com o regime de tratamento para malária não complicada. Os ataques cessam após 24 a 48 horas e os parasitas desaparecem do sangue 48 a 72 horas após o início da ingestão de cloroquina.
Para a cura radical (prevenção de recidivas remotas) da malária causada por P. vivax ou P. ovale, após o término do tratamento com cloroquina, utiliza-se um esquizontocida tecidual, a primaquina. A dose é de 0,25 mg/kg (base) por dia, durante 14 dias. Cepas de P. vivax resistentes à primaquina (as chamadas cepas do tipo Chesson) são encontradas nas ilhas do Pacífico e em países do Sudeste Asiático. Nesses casos, um dos esquemas recomendados é o uso de primaquina na dose de 0,25 mg/kg por dia, durante 21 dias.
Se P. falciparum for detectado no sangue de indivíduos não imunes em casos leves, os medicamentos de escolha, de acordo com as recomendações da OMS, são mefloquina e derivados de artemisinina (arteméter, artesunato, arteéter); halofantrina também pode ser usada. Na ausência de mefloquina e halofantrina e/ou na presença de contraindicações ao uso desses medicamentos, a quinina é prescrita em combinação com antibióticos (tetraciclina, doxiciclina). A tetraciclina é tomada 0,5 g duas vezes ao dia por 7 a 10 dias; pode ser substituída por doxiciclina em uma dose diária de 0,1 g, a duração da administração é de 7 a 10 dias. Em regiões onde P. falciparum é resistente à mefloquina e à quinina, uma combinação de preparações de mefloquina e artemisinina (artesnato, arteméter) é recomendada para o tratamento da malária tropical não complicada. A combinação de fansidar e artesunato é eficaz no tratamento da malária tropical não complicada. Preparações de artemisinina são amplamente utilizadas no tratamento da malária tropical multirresistente no Sudeste Asiático, em diversos países da América do Sul e na África. Agem muito rapidamente tanto nas células sanguíneas quanto nos gametócitos. No entanto, esses medicamentos são rapidamente eliminados do organismo, o que causa recidivas da malária. É mais apropriado prescrevê-los em combinação com mefloquina nas seguintes doses:
- artesunato: 4 mg/kg duas vezes ao dia durante 3 dias; mefloquina: 15 mg/kg uma vez no dia 2 ou 25 mg/kg em duas doses nos dias 2 e 3;
- arteméter: 3,2 mg/kg uma vez ao dia durante 3 dias; mefloquina: 15 mg/kg uma vez no dia 2 ou 25 mg/kg em duas doses nos dias 2 e 3.
Regimes de tratamento para malária não complicada
Esquemas de aplicação |
|||
Preparação |
Primeira dose, mg/kg |
Doses subsequentes, mg/kg (intervalo, h) |
Duração do curso, dias |
Cloroquina |
10 (motivos) |
10- 1-2 dias 5 - 3 dias |
3 |
Fansidar (sulfadoxina + pirimetamina) |
2,50-1,25 |
- |
1 |
Quinino, Kinimax, Kinoform |
10 (motivos) |
7,5 (8) |
7-10 |
Mefloquina |
15 (terrenos) |
- |
1 |
Halofantrina |
8 (sal) |
8 (6) |
1 |
Artesunato |
4 |
2 (12) |
7 |
Arteméter |
3.2 |
1.6 (24) |
7.0 |
Quinino-tetraciclina |
10,0-1,5 |
10,0 (8)+5,0 (6) |
10,0+7,0 |
Coartem (arteméter + lumefantrina) |
1,3+8 0 |
1,3-8,0 (8) |
3.0 |
Quando o tipo de patógeno não for estabelecido, recomenda-se que o tratamento seja realizado de acordo com os regimes de tratamento para malária tropical. Se o paciente vomitar antes de 30 minutos após tomar o medicamento antimalárico prescrito, a mesma dose deve ser administrada novamente. Se o vômito ocorrer 30 a 60 minutos após a ingestão dos comprimidos, metade da dose do medicamento será prescrita adicionalmente.
Pacientes com malária tropical grave devem ser hospitalizados em uma unidade de terapia intensiva ou departamento de ressuscitação. A quinina continua sendo o medicamento de escolha para o tratamento da malária tropical grave. No tratamento de formas complicadas (malária cerebral, álgida), a primeira dose (7 mg/kg) de base de quinina é administrada por via intravenosa durante 30 minutos. Em seguida, outros 10 mg/kg são administrados por via intravenosa por gotejamento durante 4 horas. Assim, o paciente recebe 17 mg/kg de base de quinina durante as primeiras 4,5 horas após o início do tratamento. De acordo com outro esquema, a dose inicial de 20 mg/kg de base de quinina é administrada durante 4 horas. Ambos os esquemas são tolerados satisfatoriamente pelos pacientes - sem distúrbios cardiovasculares ou outros. Uma dose de manutenção de 10 mg/kg de base de quinina é administrada em intervalos de 8 horas, a duração da administração é de 1,5 a 2 horas. É aconselhável combinar quinina com tetraciclina (250 mg quatro vezes ao dia durante 7 dias) ou doxiciclina (0,1 g por dia durante 7 a 10 dias). Para o tratamento de crianças, recomenda-se administrar uma dose de ataque (15 mg/kg) de quinina base por via intravenosa, gota a gota, em solução de glicose a 5%, durante 4 horas. Uma dose de manutenção (10 mg/kg) é administrada durante 2 horas, em intervalos de 12 horas. A mesma dose é utilizada para administração intramuscular, mas recomenda-se que a quinina seja diluída cinco vezes em água destilada e dividida em duas injeções em nádegas diferentes.
O Arteméter é usado como medicamento alternativo para o tratamento da malária tropical complicada na dose diária de 3,2 mg/kg no primeiro dia de tratamento. Nos seis dias seguintes, é administrado na dose de 1,6 mg/kg por via intramuscular em combinação com uma dose de mefloquina.
Pacientes com formas graves e complicadas de malária recebem terapia patogênica intensiva. Ao realizar a reidratação, deve-se ter cuidado com edema pulmonar e cerebral, mas a hipovolemia não é menos perigosa. Se a reidratação não for bem-sucedida, esses pacientes podem apresentar insuficiência de perfusão tecidual, acidose, hipotensão, choque e insuficiência renal. O desenvolvimento de anemia geralmente não representa risco de vida, mas se o hematócrito for reduzido para 15-20%, hemácias ou sangue total devem ser transfundidos. A transfusão de sangue total fresco ou concentrados de fatores de coagulação e plaquetas é utilizada na síndrome da coagulação intravascular disseminada (CID). Em caso de hipoglicemia, deve-se utilizar a administração intravenosa de uma solução de glicose a 40%.
A base do tratamento do edema cerebral é a desintoxicação, a desidratação, o controle da hipóxia cerebral e dos distúrbios respiratórios (oxigenoterapia, ventilação artificial). Anticonvulsivantes são administrados conforme indicado. A experiência no tratamento da malária cerebral comprovou a ineficácia e até mesmo o perigo do uso de diuréticos osmóticos: dextranos de baixo peso molecular; adrenalina; prostaciclina; pentoxifilina; ciclosporina; soros hiperimunes. A oxigenação hiperbárica também não é recomendada.
Em caso de insuficiência renal aguda ou insuficiência renal-hepática aguda, a dose diária de quinina deve ser reduzida para 10 mg/kg devido ao possível acúmulo do fármaco, e as soluções devem ser administradas a uma taxa de 20 gotas por minuto. No período inicial da insuficiência renal aguda, realiza-se diurese forçada e, se não houver efeito e a azotemia aumentar, utiliza-se hemodiálise ou diálise peritoneal, que geralmente apresenta bons resultados. Em caso de febre hemoglobinúrica, o fármaco que causou a hemólise é descontinuado. Se necessário, é substituído por outros antimaláricos, sendo prescritos concomitantemente glicocorticosteroides (prednisolona 1-2 mg/kg) e terapia de desintoxicação.
Em caso de ruptura do baço, que geralmente se desenvolve em casos de aumento rápido e significativo do órgão, é indicada intervenção cirúrgica de emergência.
Para tratar recidivas de malária tropical, seleciona-se um medicamento não utilizado anteriormente ou utiliza-se o anterior, mas em combinação com outros antimaláricos. A carreia de gametas é eliminada com primaquina por 1 a 3 dias em doses terapêuticas normais.
A eficácia do tratamento da malária é monitorada através do exame de uma gota espessa de sangue com contagem de parasitemia em 1 μl. Esses exames são realizados diariamente, do 1º ao 7º dia após o início do tratamento etiotrópico. Se os parasitas desaparecerem durante esse período, exames complementares com preparações sanguíneas são realizados no 14º, 21º e 28º dia após o início do tratamento.
Avaliação de eficácia
A eficácia do tratamento etiotrópico da malária em pacientes com malária é avaliada por três parâmetros: falha precoce (FA), falha tardia (FT) e tratamento eficaz.
Após tomar um medicamento antimalárico, o paciente pode vomitar (especialmente em crianças). É importante lembrar que, se o vômito ocorrer menos de 30 minutos após a ingestão do medicamento, a mesma dose deve ser tomada novamente e, após 30 a 60 minutos, metade da dose do medicamento utilizado.
Avaliação da eficácia do tratamento da malária (OMS, 1996)
Falha precoce (FE) |
Agravamento ou persistência dos sinais clínicos da malária na presença de parasitemia durante os primeiros 3 dias do início da terapia específica |
Falha tardia (LF) |
Reaparecimento de sinais clínicos característicos da malária (incluindo o desenvolvimento de um quadro grave) na presença de parasitemia do 4º ao 14º dia do início da terapia específica |
Eficácia do tratamento |
Ausência de parasitemia após 14 dias do início da terapia específica na ausência dos critérios RN e PN |
Tratamento radical da malária
O tratamento radical da malária é realizado simultaneamente ao tratamento de interrupção ou imediatamente após ele.
- Para a prevenção de recidivas exoeritrocíticas da malária vivax e da malária ovale, com o objetivo de afetar os hipozoítos, a primaquina é prescrita na dose de 45 mg (27 mg de base) por dia (3 comprimidos) - um tratamento de 14 dias ou 6 comprimidos - uma vez por semana - durante 6 a 8 semanas (em caso de deficiência de glicose-6-fosfato desidrogenase). O medicamento tafenoquina está em ensaios clínicos - um análogo da primaquina, mas com maior eficácia clínica e menor frequência de efeitos colaterais.
- Para prevenir a transmissão da malária falciparum (afetando os gametócitos), a primaquina é usada na dose de 45 mg (27 mg de base) por dia (3 comprimidos) durante 3 dias. O tratamento é realizado em regiões endêmicas de malária tropical. Ao usar Fansidar no tratamento de pacientes que tiveram malária falciparum, a primaquina não é prescrita devido ao efeito efetivo da pirimetamina, que faz parte do Fansidar, nos gametócitos de Pl. falciparum.
O tratamento da malária falciparum grave e/ou complicada é realizado em unidades de terapia intensiva. Se a administração oral de medicamentos não for possível, a terapia parenteral é realizada com um dos seguintes medicamentos:
- dicloridrato de quinina - 10-20 mg/kg (até 2,0 g por dia) por via intravenosa em 500 ml de solução de glicose a 5%, lentamente, 2-3 vezes por dia até que o paciente se recupere de uma condição grave, depois um dos medicamentos orais de acordo com o regime de tratamento para malária falciparum não complicada;
- Em condições modernas, novos preparados à base de ervas são usados em alguns países para tratar formas graves de malária falciparum (esses preparados não são certificados na Rússia): Artemeter (Artenam) - 160 mg por via intramuscular no primeiro dia, depois 80 mg por 6 dias; Artesunato - 50 mg por via intramuscular (por via intravenosa) 2 vezes ao dia durante 7 dias; Artemisinina - 1200 mg por via intramuscular durante 7 dias.
O tratamento patogênico da malária depende da gravidade da doença e do desenvolvimento de complicações. Terapia de desintoxicação, correção da acidose metabólica, hipoglicemia, diuréticos, anti-histamínicos, glicocorticosteroides (conforme indicado), vitaminas, medicamentos cardiovasculares e outros são prescritos. Em caso de anúria, a diálise peritoneal pode ser realizada. No tratamento da febre hemoglobinúrica, os medicamentos que causaram a hemólise são inicialmente descontinuados e a transfusão de massa de hemácias é realizada.
Os convalescentes recebem alta após a conclusão de um ciclo completo de tratamento parasitológico etiotrópico (suspensão da terapia) na presença de 2 a 3 resultados negativos nos exames de sangue (gota espessa). Pacientes que tiveram malária vivax e malária ovale podem ser submetidos a um ciclo subsequente de tratamento com primaquina em regime ambulatorial. Pacientes que tiveram malária são monitorados por 1 a 1,5 mês, com testes parasitológicos repetidos de uma gota espessa de sangue a cada 7 a 10 dias. Pacientes que tiveram malária vivax, malária ovale e malária malariae são monitorados por dois anos, com testes parasitológicos obrigatórios de uma gota espessa a qualquer aumento de temperatura.
Prevenção
A OMS está combatendo a malária em todo o mundo dentro da estrutura do Programa Roll Back Malaria, adotado em 1998. Atualmente, a OMS estabeleceu uma nova meta para a Região Europeia: eliminar a malária de três dias (P. vivax) até 2010 e a malária tropical até 2015. O elo mais importante no complexo de medidas é a detecção e o tratamento oportunos das fontes de infecção.
As medidas preventivas durante o surto visam a detecção e o tratamento oportunos da malária, bem como dos portadores do parasita (fontes de infecção), bem como o combate aos portadores da malária. Atualmente, não existem vacinas eficazes para imunização ativa contra a malária.
A profilaxia individual da malária durante a permanência em um foco endêmico visa prevenir a infecção e prevenir um ataque de malária. A prevenção da infecção consiste em tomar medidas de proteção contra picadas de mosquitos (uso de repelentes, mosquiteiros em janelas e portas, cortinas de cama, roupas que cubram os braços e as pernas ao permanecer ao ar livre à noite). De acordo com as recomendações da OMS, a prevenção de um ataque de malária consiste no uso de medicamentos antimaláricos, sendo recomendada apenas para indivíduos não imunes que viajam para focos com alto risco de infecção por malária e com falta de atendimento médico acessível (distanciamento das instituições médicas, impossibilidade de testes rápidos de sangue para malária).
A necessidade, a duração e a frequência do uso dos medicamentos são determinadas somente após consulta com um infectologista. É importante identificar contraindicações para o uso de quimioterápicos e a presença de doenças concomitantes graves. Gestantes não imunes e crianças pequenas não devem visitar regiões endêmicas de malária.
Dada a alta resistência do Pl. falciparum à cloroquina, a dose padrão para a prevenção da malária falciparum, conforme recomendado pela OMS, é atualmente a mefloquina (250 mg uma vez por semana, 2 semanas antes de partir para uma região endêmica e por 4 semanas após o retorno). O uso de outros medicamentos (doxiciclina, cloroquina em combinação com proguanil, atovaquina em combinação com proguanil, primaquina e outros) é determinado por um especialista em doenças infecciosas, levando em consideração a situação epidemiológica da região de estadia e outros fatores mencionados acima.
Previsão
Na maioria dos casos, a mortalidade é causada pela malária tropical, ou mais precisamente, por sua forma cerebral, que ocorre em 10% dos casos de malária falciparum grave. Mortes por outros tipos de malária são muito raras. Mas a malária tropical, com diagnóstico oportuno e tratamento adequado, resulta em recuperação completa.
Para pacientes que tiveram malária tropical, recomenda-se estabelecer observação em dispensário por 1 a 1,5 mês e realizar exames parasitológicos de sangue em intervalos de 1 a 2 semanas. A observação em dispensário de pacientes que tiveram malária causada por P. vivax, P. ovale e P. malariae deve ser realizada por dois anos. Qualquer aumento na temperatura corporal requer exames laboratoriais de sangue para identificar prontamente os plasmódios da malária.

