Médico especialista do artigo
Novas publicações
Ovário
Última revisão: 04.07.2025

Todo o conteúdo do iLive é medicamente revisado ou verificado pelos fatos para garantir o máximo de precisão factual possível.
Temos diretrizes rigorosas de fornecimento e vinculamos apenas sites de mídia respeitáveis, instituições de pesquisa acadêmica e, sempre que possível, estudos médicos revisados por pares. Observe que os números entre parênteses ([1], [2], etc.) são links clicáveis para esses estudos.
Se você achar que algum dos nossos conteúdos é impreciso, desatualizado ou questionável, selecione-o e pressione Ctrl + Enter.
O ovário (ovário; grego oóforo) é um órgão par, uma glândula reprodutora feminina, localizada na cavidade pélvica, atrás do ligamento largo do útero. Nos ovários, as células reprodutoras femininas (óvulos) se desenvolvem e amadurecem, e os hormônios sexuais femininos são formados, os quais entram no sangue e na linfa. O ovário tem formato ovoide, um pouco achatado na direção anteroposterior. A cor do ovário é rosada. Na superfície do ovário de uma mulher que deu à luz, depressões e cicatrizes são visíveis - vestígios da ovulação e da transformação dos corpos lúteos. O ovário pesa de 5 a 8 g. As dimensões do ovário são: comprimento 2,5 a 5,5 cm, largura 1,5 a 3,0 cm, espessura - até 2 cm. O ovário possui duas superfícies livres: a face medial (fácies medial), voltada para a cavidade pélvica, parcialmente coberta pela trompa de Falópio, e a face lateral (fácies lateral), adjacente à parede lateral da pelve, a uma depressão ligeiramente pronunciada – a fossa ovariana. Esta fossa localiza-se no ângulo entre os vasos ilíacos externos, recobertos por peritônio na parte superior, e as artérias uterina e obturadora na parte inferior. Atrás do ovário, o ureter do lado correspondente passa retroperitonealmente de cima para baixo.
As superfícies do ovário passam para uma borda livre convexa (posterior) (margo liber), na frente - para a borda mesentérica (margo mesovaricus), fixada por meio de uma pequena prega do peritônio (mesentério do ovário) à cúspide posterior do ligamento largo do útero. Nesta borda anterior do órgão há uma depressão sulcada - o hilo do ovário (hilum ovarii), através do qual a artéria e os nervos entram no ovário, e as veias e os vasos linfáticos saem. O ovário também tem duas extremidades: a extremidade tubular superior arredondada (extremitas tubaria), voltada para a trompa de Falópio, e a extremidade uterina inferior (extremitas utenna), conectada ao útero pelo ligamento ovariano (lig. ovarii proprium). Este ligamento, na forma de um cordão redondo com cerca de 6 mm de espessura, vai da extremidade uterina do ovário até o ângulo lateral do útero, localizado entre as duas folhas do ligamento largo do útero. O aparelho ligamentar do ovário também inclui o ligamento suspensor do ovário (lig.suspensorium ovarii), que é uma prega do peritônio que se estende da parede da pequena pelve até o ovário e contém os vasos ovarianos e feixes de fibras fibrosas em seu interior. O ovário é fixado por um mesentério curto (mesovário), que é uma duplicação do peritônio que se estende da cúspide posterior do ligamento largo do útero até a borda mesentérica do ovário. Os ovários em si não são cobertos pelo peritônio. A maior franja ovariana da trompa de Falópio está fixada à extremidade tubular do ovário. A topografia do ovário depende da posição do útero e do seu tamanho (durante a gravidez). Os ovários são órgãos muito móveis da cavidade pélvica.
Vasos e nervos do ovário
O suprimento sanguíneo para os ovários é fornecido por aa. et vv. ovaricae et uterinae. Ambas as artérias ovarianas (aa. ovaricae dextra et sinistra) se originam da superfície anterior da aorta, logo abaixo das artérias renais; a direita geralmente se origina da aorta, e a esquerda da artéria renal. Direcionando-se para baixo e lateralmente ao longo da superfície anterior do músculo psoas maior, cada artéria ovariana cruza o ureter na frente (emitindo ramos para ele), os vasos ilíacos externos, a linha de borda e entra na cavidade pélvica, estando localizada aqui no ligamento suspensor do ovário. Seguindo na direção medial, a artéria ovariana passa entre as folhas do ligamento largo do útero sob a trompa de Falópio, emitindo ramos para ela, e então para o mesentério do ovário; ela entra no hilo do ovário.
Os ramos da artéria ovariana anastomosam-se amplamente com os ramos ovarianos da artéria uterina. O fluxo venoso dos ovários é realizado principalmente para o plexo venoso ovariano, localizado na região do hilo ovariano. A partir daí, o fluxo sanguíneo ocorre em duas direções: através das veias uterina e ovariana. A veia ovariana direita possui válvulas e desemboca na veia cava inferior. A veia ovariana esquerda desemboca na veia renal esquerda, embora não possua válvulas.
A drenagem linfática dos ovários ocorre através dos vasos linfáticos, especialmente abundantemente na região da porta de entrada dos órgãos, onde se distingue o plexo linfático subovariano. Em seguida, a linfa é drenada ao longo dos vasos linfáticos ovarianos para os linfonodos para-aórticos.
Inervação dos ovários
Simpático - fornecido por fibras pós-ganglionares dos plexos celíaco (solar), mesentérico superior e hipogástrico; parassimpático - pelos nervos sacrais viscerais.
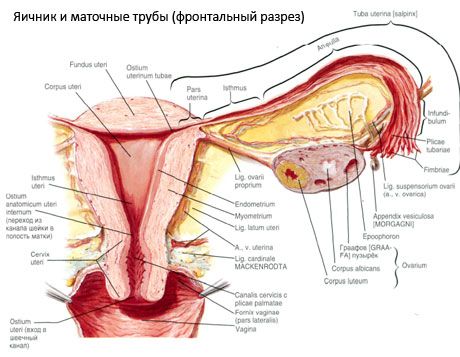
Estrutura do ovário
A superfície do ovário é revestida por um epitélio germinativo de camada única. Abaixo dele, encontra-se uma densa camada de tecido conjuntivo proteico (túnica albugínea). O tecido conjuntivo do ovário forma seu estroma (stroma ovarii), rico em fibras elásticas. A substância do ovário, seu parênquima, é dividida em camadas externa e interna. A camada interna, localizada no centro do ovário, mais próxima de sua entrada, é chamada de medula ovarii. Nessa camada, em tecido conjuntivo frouxo, existem numerosos vasos sanguíneos e linfáticos e nervos. A camada externa do ovário - o córtex (cortex ovarii) - é mais densa. Contém muito tecido conjuntivo, no qual estão localizados os folículos ovarianos primários em maturação (folliculi ovarici primarii), folículos secundários (vesiculares) (folliculi ovarici secundarii, s.vesiculosi), bem como folículos maduros, folículos de Graaf (folliculi ovarici maturis), bem como corpos amarelos e atrésicos.
Cada folículo contém um óvulo reprodutor feminino, ou ovócito (ovócitos). O óvulo tem até 150 µm de diâmetro, é redondo, contém um núcleo, uma grande quantidade de citoplasma, que, além de organelas celulares, contém inclusões proteico-lipídicas (gema) e glicogênio, necessários para a nutrição do óvulo. O óvulo geralmente esgota seu suprimento de nutrientes dentro de 12 a 24 horas após a ovulação. Se a fertilização não ocorrer, o óvulo morre.
O óvulo humano é revestido por duas membranas. Dentro dele está o citolema, que é a membrana citoplasmática do óvulo. Do lado de fora do citolema, há uma camada de células foliculares, que protegem o óvulo e desempenham uma função de formação de hormônios — elas secretam estrogênios.
A posição fisiológica do útero, das trompas e dos ovários é assegurada pelos aparelhos de suspensão, fixação e suporte que unem o peritônio, os ligamentos e o tecido pélvico. O aparelho de suspensão é representado por formações pareadas e inclui os ligamentos redondo e largo do útero, os ligamentos próprios e os ligamentos de suspensão dos ovários. Os ligamentos largos do útero, os ligamentos próprios e os ligamentos de suspensão dos ovários mantêm o útero na posição intermediária. Os ligamentos redondos puxam o fundo do útero para a frente e proporcionam sua inclinação fisiológica.
O aparelho de fixação (ancoragem) garante a posição do útero no centro da pequena pelve e torna praticamente impossível seu deslocamento para os lados, para frente e para trás. No entanto, como o aparelho ligamentar se afasta do útero em sua parte inferior, é possível que o útero se incline em várias direções. O aparelho de fixação inclui ligamentos localizados no tecido frouxo da pelve e que se estendem da parte inferior do útero até as paredes lateral, anterior e posterior da pelve: ligamentos sacro-mágico, cardinal, uterovesical e vesicopúbico.
Além do mesovário, distinguem-se os seguintes ligamentos ovarianos:
- o ligamento suspensor do ovário, anteriormente designado como ligamento infundibulopélvico. É uma prega do peritônio por onde passam vasos sanguíneos (a. et v. ovarica) e vasos linfáticos e nervos do ovário, esticada entre a parede lateral da pelve, a fáscia lombar (na área de divisão da artéria ilíaca comum em externa e interna) e a extremidade superior (tubária) do ovário;
- O ligamento próprio do ovário passa entre as lâminas do ligamento uterino largo, mais próximo da lâmina posterior, e conecta a extremidade inferior do ovário com a borda lateral do útero. O ligamento próprio do ovário insere-se no útero entre o início da trompa de Falópio e o ligamento redondo, atrás e acima deste último. Na espessura do ligamento passam os rr. ovarii, que são os ramos terminais da artéria uterina;
- Ligamento apendicular-ovariano. Estende-se do mesentério do apêndice até o ovário direito ou ligamento largo do útero, formando uma prega do peritônio. O ligamento é instável e é observado em 1/2 a 1/3 das mulheres.
O aparelho de suporte é representado pelos músculos e fáscias do assoalho pélvico, divididos em camadas inferior, média e superior (interna).
A mais potente é a camada muscular superior (interna), representada pelo par de músculos que levanta o ânus. Ela consiste em feixes musculares que se estendem do cóccix até os ossos pélvicos em três direções (pubococcígeo, iliococcígeo e isquiococcígeo). Essa camada de músculos também é chamada de diafragma pélvico.
A camada média de músculos está localizada entre a sínfise e os ossos púbico e isquiático. A camada média de músculos – o diafragma urogenital – ocupa a metade anterior da saída pélvica, por onde passam a uretra e a vagina. Na parte anterior, entre suas lâminas, encontram-se feixes musculares que formam o esfíncter externo da uretra; na parte posterior, feixes musculares que se estendem na direção transversal – o músculo transverso profundo do períneo.
A camada inferior (externa) dos músculos do assoalho pélvico consiste em músculos superficiais, cujo formato lembra o número 8. Eles incluem o bulbocavernoso, o isquiocavernoso, o esfíncter anal externo e o músculo transverso superficial do períneo.
Ontogênese dos ovários
O processo de crescimento folicular e atresia começa na 20ª semana de gestação e, no momento do parto, até 2 milhões de ovócitos permanecem nos ovários da menina. Na menarca, seu número diminui para 300 mil. Durante todo o período da vida reprodutiva, não mais do que 500 folículos atingem a maturidade e ovulam. O crescimento inicial dos folículos não depende da estimulação do FSH, é limitado e a atresia ocorre rapidamente. Acredita-se que, em vez de hormônios esteroides, os peptídeos autócrinos/parácrinos locais sejam o principal regulador do crescimento e da atresia dos folículos primários. Acredita-se que o processo de crescimento folicular e atresia não seja interrompido por nenhum processo fisiológico. Esse processo continua em todas as idades, incluindo o período intrauterino e a menopausa, e é interrompido pela gestação, ovulação e anovulação. O mecanismo que desencadeia o crescimento folicular e seu número em cada ciclo específico ainda não está claro.
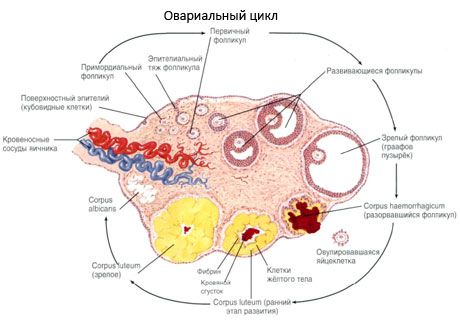
Durante seu desenvolvimento, o folículo passa por vários estágios. As células germinativas primordiais originam-se do endoderma do saco vitelínico, alantoide, e migram para a área genital do embrião entre 5 e 6 semanas de gestação. Como resultado da rápida divisão mitótica, que continua entre 6 e 8 semanas e 16 e 20 semanas de gestação, até 6 a 7 milhões de ovócitos são formados nos ovários do embrião, circundados por uma fina camada de células da granulosa.
Folículo pré-antral - o ovócito é envolvido por uma membrana (zona pelúcida). As células da granulosa que circundam o ovócito começam a proliferar, seu crescimento depende de gonadotrofinas e se correlaciona com os níveis de estrogênio. As células da granulosa são o alvo do FSH. No estágio do folículo pré-antral, as células da granulosa são capazes de sintetizar três classes de esteroides: predominantemente, induz a atividade da aromatase, a principal enzima que converte andrógenos em estradiol. Acredita-se que o estradiol seja capaz de aumentar o número de seus próprios receptores, exercendo um efeito mitogênico direto sobre as células da granulosa, independente do FSH. É considerado um fator parácrino que potencializa os efeitos do FSH, incluindo a ativação dos processos de aromatização.
Os receptores de FSH aparecem nas membranas das células da granulosa assim que o crescimento folicular se inicia. Uma diminuição ou aumento do FSH leva a uma alteração no número de seus receptores. Essa ação do FSH é modulada por fatores de crescimento. O FSH atua por meio da proteína G, o sistema adenilato ciclase. Embora a esteroidogênese no folículo seja regulada principalmente pelo FSH, muitos fatores estão envolvidos nesse processo: canais iônicos, receptores de tirosina quinase e o sistema fosfolipase de segundos mensageiros.
O papel dos andrógenos no desenvolvimento folicular inicial é complexo. As células da granulosa possuem receptores de andrógenos. Estes não são apenas um substrato para a aromatização induzida por FSH em estrogênios, mas também podem aumentar a aromatização em baixas concentrações. Quando os níveis de andrógenos aumentam, as células da granulosa pré-antral escolhem preferencialmente não a via de aromatização para estrogênios, mas a via androgênica mais simples, via 5a-redutase, para converter em um andrógeno que não pode ser convertido em estrogênio, inibindo assim a atividade da aromatase. Esse processo também inibe a formação dos receptores de FSH e LH, interrompendo o desenvolvimento folicular.
No processo de aromatização, o folículo com altos níveis de andrógenos sofre processos de atresia. O crescimento e o desenvolvimento do folículo dependem de sua capacidade de converter andrógenos em estrogênios.
Na presença de FSH, a substância dominante no fluido folicular será o estrogênio. Na ausência de FSH, os andrógenos. O LH normalmente está ausente no fluido folicular até a metade do ciclo. Assim que o nível de LH aumenta, a atividade mitótica das células da granulosa diminui, surgem alterações degenerativas e o nível de andrógeno no folículo aumenta. O nível de esteroides no fluido folicular é maior do que no plasma e reflete a atividade funcional das células ovarianas: células da granulosa e da teca. Se o único alvo do FSH são as células da granulosa, então o LH tem muitos alvos - células da teca, células estromais e luteínicas e células da granulosa. Tanto as células da granulosa quanto as da teca têm a capacidade de esteroidogênese, mas a atividade da aromatase predomina nas células da granulosa.
Em resposta ao LH, as células da teca produzem andrógenos, que são então convertidos pelas células da granulosa em estrogênios por meio da aromatização induzida por FSH.
À medida que o folículo cresce, as células da teca começam a expressar genes para receptores de LH, P450 seg e 3beta-hidroxiesteroide desidrogenase, fator de crescimento semelhante à insulina (IGF-1) sinergicamente com LH aumenta a expressão genética, mas não estimula a esteroidogênese.
A esteroidogênese ovariana é sempre dependente de LH. À medida que o folículo cresce, as células da teca expressam a enzima P450c17, que forma andrógenos a partir do colesterol. As células da granulosa não possuem essa enzima e dependem das células da teca para produzir estrogênios a partir de andrógenos. Ao contrário da esteroidogênese, a foliculogênese é dependente de FSH. À medida que o folículo cresce e os níveis de estrogênio aumentam, um mecanismo de feedback é ativado: a produção de FSH é inibida, o que, por sua vez, leva à diminuição da atividade da aromatase do folículo e, por fim, à atresia folicular por apoptose (morte celular programada).
O mecanismo de feedback dos estrogênios e do FSH inibe o desenvolvimento dos folículos que começaram a crescer, mas não o folículo dominante. O folículo dominante contém mais receptores de FSH, que auxiliam na proliferação das células da granulosa e na aromatização dos andrógenos em estrogênios. Além disso, as vias parácrinas e autócrinas atuam como importantes coordenadoras do desenvolvimento do folículo antral.
O regulador autócrino/parácrino consiste em peptídeos (inibina, activina, folistatina), que são sintetizados pelas células da granulosa em resposta ao FSH e entram no fluido folicular. A inibina reduz a secreção de FSH; a activina estimula a liberação de FSH pela hipófise e potencializa a ação do FSH no ovário; a folistatina suprime a atividade do FSH, possivelmente pela ligação à activina. Após a ovulação e o desenvolvimento do corpo lúteo, a inibina fica sob o controle do LH.
O crescimento e a diferenciação das células ovarianas são influenciados por fatores de crescimento semelhantes à insulina (IGE). O IGF-1 atua nas células da granulosa, causando um aumento nos níveis de monofosfato de adenosina cíclico (AMPc), progesterona, ocitocina, proteoglicano e inibina.
O IGF-1 atua nas células da teca, causando aumento na produção de andrógenos. As células da teca, por sua vez, produzem fator de necrose tumoral (TNF) e fator de crescimento epidérmico (EGF), que também são regulados pelo FSH.
O EGF estimula a proliferação de células da granulosa. O IGF-2 é o principal fator de crescimento no fluido folicular, e IGF-1, TNF-a, TNF-3 e EGF também são encontrados nele.
A interrupção da regulação parácrina e/ou autócrina da função ovariana parece desempenhar um papel nos distúrbios da ovulação e no desenvolvimento de ovários policísticos.
À medida que o folículo antral cresce, o conteúdo de estrogênio no fluido folicular aumenta. No pico desse aumento, receptores de LH aparecem nas células da granulosa, ocorre a luteinização das células da granulosa e a produção de progesterona aumenta. Assim, no período pré-ovulatório, um aumento na produção de estrogênio causa o surgimento de receptores de LH, que, por sua vez, causam a luteinização das células da granulosa e a produção de progesterona. Um aumento na progesterona reduz os níveis de estrogênio, o que aparentemente causa um segundo pico de FSH no meio do ciclo.
Acredita-se que a ovulação ocorra de 10 a 12 horas após o pico de LH e de 24 a 36 horas após o pico de estradiol. Acredita-se que o LH estimule a divisão redutora do ovócito, a luteinização das células da granulosa e a síntese de progesterona e prostaglandina no folículo.
A progesterona aumenta a atividade de enzimas proteolíticas, que, juntamente com a prostaglandina, participam da ruptura da parede folicular. O pico de FSH induzido pela progesterona permite que o ovócito saia do folículo convertendo o plasminogênio na enzima proteolítica plasmina, e fornece um número suficiente de receptores de LH para o desenvolvimento normal da fase lútea.
Dentro de 3 dias após a ovulação, as células da granulosa aumentam de tamanho e nelas aparecem vacúolos característicos, preenchidos com o pigmento luteína. As células teca-lúteas diferenciam-se da teca e do estroma e tornam-se parte do corpo lúteo. Os capilares que penetram o corpo lúteo desenvolvem-se muito rapidamente sob a influência de fatores angiogênicos e, com a melhora da vascularização, a produção de progesterona e estrogênios aumenta. A atividade da esteroidogênese e a longevidade do corpo lúteo são determinadas pelos níveis de LH. O corpo lúteo não é uma formação celular homogênea. Além de dois tipos de células luteais, ele contém células endoteliais, macrófagos, fibroblastos, etc. As células luteais grandes produzem peptídeos (relaxina, ocitocina) e são mais ativas na esteroidogênese, com maior atividade da aromatase e maior síntese de progesterona do que as células pequenas.
O pico de progesterona ocorre no 8º dia após o pico de LH. Observa-se que a progesterona e o estradiol são secretados episodicamente na fase lútea, em correlação com a produção pulsátil de LH. Com a formação do corpo lúteo, o controle da produção de inibina passa do FSH para o LH. A inibina aumenta com o aumento do estradiol antes do pico de LH e continua a aumentar após o pico de LH, embora os níveis de estrogênio diminuam. Embora a inibina e o estradiol sejam secretados pelas células da granulosa, eles são regulados por vias diferentes. O declínio da inibina no final da fase lútea contribui para o aumento do FSH para o próximo ciclo.
O corpo lúteo diminui muito rapidamente - no 9º ao 11º dia após a ovulação.
O mecanismo de degeneração não é claro e não está relacionado ao papel luteolítico dos estrogênios ou a um mecanismo relacionado a receptores, como observado no endométrio. Há outra explicação para o papel dos estrogênios produzidos pelo corpo lúteo. Sabe-se que os estrogênios são necessários para a síntese de receptores de progesterona no endométrio. Os estrogênios da fase lútea são provavelmente necessários para as alterações relacionadas à progesterona no endométrio após a ovulação. O desenvolvimento inadequado dos receptores de progesterona, como consequência de níveis inadequados de estrogênio, é possivelmente um mecanismo adicional para infertilidade e perdas gestacionais precoces, outra forma de deficiência da fase lútea. Acredita-se que a vida útil do corpo lúteo seja estabelecida no momento da ovulação. E certamente regredirá se não for sustentado pela gonadotrofina coriônica humana devido à gravidez. Assim, a regressão do corpo lúteo leva a uma diminuição nos níveis de estradiol, progesterona e inibina. A diminuição da inibina remove seu efeito supressor sobre o FSH; a diminuição do estradiol e da progesterona permite uma restauração muito rápida da secreção de GnRH e a remoção do mecanismo de feedback da hipófise. A diminuição da inibina e do estradiol, juntamente com o aumento do GnRH, dá origem ao FSH em detrimento do LH. O aumento do FSH leva ao crescimento folicular com a subsequente seleção de um folículo dominante, iniciando-se um novo ciclo se a gravidez não ocorrer. Os hormônios esteroides desempenham um papel fundamental na biologia reprodutiva e na fisiologia geral. Eles determinam o fenótipo humano, afetam o sistema cardiovascular, o metabolismo ósseo, a pele, o bem-estar geral e desempenham um papel fundamental na gravidez. A ação dos hormônios esteroides reflete os mecanismos intracelulares e genéticos necessários para transmitir um sinal extracelular ao núcleo da célula e causar uma resposta fisiológica.
Os estrogênios penetram difusamente na membrana celular e se ligam a receptores localizados no núcleo da célula. O complexo receptor-esteroide então se liga ao DNA. Nas células-alvo, essas interações levam à expressão gênica, à síntese proteica e à função específica de células e tecidos.


 [
[