Médico especialista do artigo
Novas publicações
Diagnóstico da osteoartrose: ressonância magnética
Última revisão: 04.07.2025

Todo o conteúdo do iLive é medicamente revisado ou verificado pelos fatos para garantir o máximo de precisão factual possível.
Temos diretrizes rigorosas de fornecimento e vinculamos apenas sites de mídia respeitáveis, instituições de pesquisa acadêmica e, sempre que possível, estudos médicos revisados por pares. Observe que os números entre parênteses ([1], [2], etc.) são links clicáveis para esses estudos.
Se você achar que algum dos nossos conteúdos é impreciso, desatualizado ou questionável, selecione-o e pressione Ctrl + Enter.
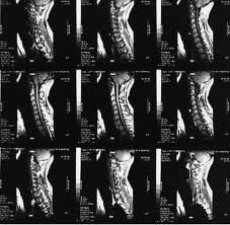
A ressonância magnética (RM) tornou-se um dos principais métodos de diagnóstico não invasivo da osteoartrite nos últimos anos. Desde a década de 1970, quando os princípios da ressonância magnética (RM) foram utilizados pela primeira vez para estudar o corpo humano, esse método de imagem médica mudou drasticamente e continua a evoluir rapidamente.
Equipamentos técnicos e softwares estão sendo aprimorados, métodos de aquisição de imagens estão sendo desenvolvidos e agentes de contraste para ressonância magnética estão sendo desenvolvidos. Isso permite que novas áreas de aplicação para a ressonância magnética sejam constantemente descobertas. Se a princípio sua aplicação se limitava a estudos do sistema nervoso central, hoje a ressonância magnética é usada com sucesso em quase todas as áreas da medicina.
Em 1946, grupos de pesquisadores das Universidades de Stanford e Harvard descobriram, de forma independente, um fenômeno chamado ressonância magnética nuclear (RMN). Sua essência era que os núcleos de alguns átomos, estando em um campo magnético, sob a influência de um campo eletromagnético externo, são capazes de absorver energia e então emiti-la na forma de um sinal de rádio. Por essa descoberta, F. Bloch e E. Parmel receberam o Prêmio Nobel em 1952. O novo fenômeno foi logo usado para análise espectral de estruturas biológicas (espectroscopia de RMN). Em 1973, Paul Rautenburg demonstrou pela primeira vez a possibilidade de obter uma imagem usando sinais de RMN. Foi assim que surgiu a tomografia de RMN. Os primeiros tomogramas de RMN dos órgãos internos de uma pessoa viva foram demonstrados em 1982 no Congresso Internacional de Radiologistas em Paris.
Dois esclarecimentos devem ser feitos. Apesar de o método ser baseado no fenômeno da RMN, ele é chamado de ressonância magnética (RM), omitindo a palavra "nuclear". Isso é feito para que os pacientes não tenham pensamentos sobre a radioatividade associada ao decaimento dos núcleos atômicos. E a segunda circunstância: os tomógrafos de RM não são acidentalmente "sintonizados" para prótons, ou seja, núcleos de hidrogênio. Há uma grande quantidade desse elemento nos tecidos, e seus núcleos têm o maior momento magnético entre todos os núcleos atômicos, o que determina um nível bastante alto de sinal de RM.
Se em 1983 havia apenas alguns dispositivos adequados para pesquisa clínica no mundo, no início de 1996 havia cerca de 10.000 tomógrafos em operação em todo o mundo. A cada ano, 1.000 novos dispositivos são introduzidos na prática. Mais de 90% do parque de tomógrafos de ressonância magnética são modelos com ímãs supercondutores (0,5-1,5 T). É interessante notar que, se em meados da década de 80 as empresas fabricantes de tomógrafos de ressonância magnética se guiavam pelo princípio "quanto maior o campo, melhor", concentrando-se em modelos com campo de 1,5 T ou mais, no final da década de 80 ficou claro que, na maioria das áreas de aplicação, eles não apresentavam vantagens significativas sobre os modelos com intensidade de campo média. Portanto, os principais fabricantes de tomógrafos de ressonância magnética (General Electric, Siemens, Philips, Toshiba, Picker, Bruker, etc.) estão atualmente dedicando grande atenção à produção de modelos com campos médios e até baixos, que se diferenciam dos sistemas de alto campo por sua compacidade e economia, com qualidade de imagem satisfatória e custo significativamente menor. Os sistemas de alto campo são utilizados principalmente em centros de pesquisa para espectroscopia de ressonância magnética.
Princípio do método de ressonância magnética
Os principais componentes de um aparelho de ressonância magnética são: um ímã superforte, um transmissor de rádio, uma bobina receptora de radiofrequência, um computador e um painel de controle. A maioria dos aparelhos possui um campo magnético com momento magnético paralelo ao eixo longitudinal do corpo humano. A intensidade do campo magnético é medida em teslas (T). Para ressonância magnética clínica, são utilizados campos com intensidade de 0,2 a 1,5 T.
Quando um paciente é colocado em um forte campo magnético, todos os prótons, que são dipolos magnéticos, giram na direção do campo externo (como uma agulha de bússola orientada para o campo magnético da Terra). Além disso, os eixos magnéticos de cada próton começam a girar em torno da direção do campo magnético externo. Esse movimento rotacional específico é chamado de procissão, e sua frequência é chamada de frequência de ressonância. Quando pulsos curtos de radiofrequência eletromagnética são passados através do corpo do paciente, o campo magnético das ondas de rádio faz com que os momentos magnéticos de todos os prótons girem em torno do momento magnético do campo externo. Para que isso aconteça, a frequência das ondas de rádio deve ser igual à frequência de ressonância dos prótons. Esse fenômeno é chamado de ressonância magnética. Para mudar a orientação dos prótons magnéticos, os campos magnéticos dos prótons e das ondas de rádio devem ressoar, ou seja, ter a mesma frequência.
Um momento magnético líquido é criado nos tecidos do paciente: os tecidos são magnetizados e seu magnetismo é orientado estritamente paralelo ao campo magnético externo. O magnetismo é proporcional ao número de prótons por unidade de volume de tecido. O enorme número de prótons (núcleos de hidrogênio) contidos na maioria dos tecidos significa que o momento magnético líquido é grande o suficiente para induzir uma corrente elétrica em uma bobina receptora localizada fora do paciente. Esses sinais de RM induzidos são usados para reconstruir a imagem de RM.
O processo de transição dos elétrons do núcleo do estado excitado para o estado de equilíbrio é chamado de processo de relaxação spin-rede ou relaxação longitudinal. É caracterizado por T1 - o tempo de relaxação spin-rede - o tempo necessário para transferir 63% dos núcleos para o estado de equilíbrio após sua excitação por um pulso de 90°. T2 - o tempo de relaxação spin-spin também é diferenciado.
Existem vários métodos para obter tomogramas de RM. Eles diferem na ordem e na natureza da geração do pulso de radiofrequência e nos métodos de análise do sinal de RM. Os dois métodos mais utilizados são o spin-lattice e o spin-eco. O spin-lattice analisa principalmente o tempo de relaxamento T1. Diferentes tecidos (substância cinzenta e branca do cérebro, líquido cefalorraquidiano, tecido tumoral, cartilagem, músculos, etc.) contêm prótons com diferentes tempos de relaxamento T1. A intensidade do sinal de RM está relacionada à duração de T1: quanto menor o T1, mais intenso o sinal de RM e mais brilhante a área da imagem aparece no monitor de TV. O tecido adiposo é branco nos tomogramas de RM, seguido pelo cérebro e medula espinhal, órgãos internos densos, paredes vasculares e músculos em ordem decrescente de intensidade do sinal de RM. Ar, ossos e calcificações praticamente não produzem um sinal de RM e, portanto, são exibidos em preto. Essas relações de tempo de relaxamento T1 criam os pré-requisitos para a visualização de tecidos normais e alterados em exames de RM.
Em outro método de ressonância magnética, chamado spin-eco, uma série de pulsos de radiofrequência é direcionada ao paciente, girando os prótons em precessão em 90°. Após a cessação dos pulsos, os sinais de resposta da ressonância magnética são registrados. No entanto, a intensidade do sinal de resposta está relacionada de forma diferente à duração do T2: quanto menor o T2, mais fraco o sinal e, consequentemente, menor o brilho na tela do monitor de TV. Assim, a imagem final da ressonância magnética usando o método T2 é o oposto daquela usando o método T1 (assim como um negativo é o oposto de um positivo).
As tomografias por ressonância magnética (RM) mostram melhor os tecidos moles do que as tomografias computadorizadas: músculos, camadas de gordura, cartilagem e vasos sanguíneos. Alguns aparelhos podem produzir imagens dos vasos sanguíneos sem a injeção de contraste (angiografia por RM). Devido ao baixo teor de água no tecido ósseo, este não cria um efeito de blindagem, como na tomografia computadorizada de raios X, ou seja, não interfere na imagem, por exemplo, da medula espinhal, dos discos intervertebrais, etc. É claro que os núcleos de hidrogênio não estão contidos apenas na água, mas no tecido ósseo eles estão fixados em moléculas muito grandes e estruturas densas e não interferem na RM.
Vantagens e desvantagens da ressonância magnética
As principais vantagens da ressonância magnética incluem a não invasividade, a ausência de exposição à radiação, a natureza tridimensional da aquisição de imagens, o contraste natural do sangue em movimento, a ausência de artefatos no tecido ósseo, a alta diferenciação de tecidos moles e a capacidade de realizar espectroscopia de MP para estudos in vivo do metabolismo tecidual. A ressonância magnética permite a obtenção de imagens de finas camadas do corpo humano em qualquer corte – nos planos frontal, sagital, axial e oblíquo. É possível reconstruir imagens volumétricas de órgãos e sincronizar a aquisição de tomogramas com os dentes do eletrocardiograma.
As principais desvantagens geralmente incluem o tempo relativamente longo necessário para obter imagens (geralmente minutos), o que leva ao aparecimento de artefatos dos movimentos respiratórios (isso reduz especialmente a eficácia do exame pulmonar), arritmias (no exame cardíaco), a incapacidade de detectar com segurança cálculos, calcificações, alguns tipos de patologia óssea, o alto custo do equipamento e sua operação, requisitos especiais para as instalações nas quais os dispositivos estão localizados (blindagem contra interferências), a incapacidade de examinar pacientes com claustrofobia, marcapassos artificiais, grandes implantes metálicos feitos de metais não médicos.
 [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ]
[ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ]
Agentes de contraste para ressonância magnética
No início do uso da ressonância magnética, acreditava-se que o contraste natural entre diferentes tecidos eliminava a necessidade de agentes de contraste. Logo se descobriu que a diferença de sinais entre diferentes tecidos, ou seja, o contraste da imagem de ressonância magnética, poderia ser significativamente melhorada por agentes de contraste. Quando o primeiro agente de contraste para ressonância magnética (contendo íons paramagnéticos de gadolínio) se tornou comercialmente disponível, o conteúdo de informação diagnóstica da ressonância magnética aumentou significativamente. A essência do uso de agentes de contraste para ressonância magnética é alterar os parâmetros magnéticos dos prótons de tecidos e órgãos, ou seja, alterar o tempo de relaxamento (TR) dos prótons T1 e T2. Hoje, existem várias classificações de agentes de contraste para ressonância magnética (ou melhor, agentes de contraste - CA).
De acordo com o efeito predominante no tempo de relaxamento, o MR-KA é dividido em:
- T1-CA, que encurtam o T1 e, portanto, aumentam a intensidade do sinal de MP tecidual. Também são chamados de CA positivos.
- CAs de T2 que encurtam o T2, reduzindo a intensidade do sinal de RM. São CAs negativos.
Dependendo de suas propriedades magnéticas, os MR-CA são divididos em paramagnéticos e superparamagnéticos:
 [ 16 ], [ 17 ], [ 18 ], [ 19 ], [ 20 ]
[ 16 ], [ 17 ], [ 18 ], [ 19 ], [ 20 ]
Agentes de contraste paramagnéticos
Propriedades paramagnéticas são possuídas por átomos com um ou mais elétrons desemparelhados. São íons magnéticos de gadolínio (Gd), cromo, níquel, ferro e manganês. Os compostos de gadolínio têm recebido a mais ampla aplicação clínica. O efeito de contraste do gadolínio se deve ao encurtamento dos tempos de relaxação T1 e T2. Em baixas doses, o efeito em T1 predomina, aumentando a intensidade do sinal. Em altas doses, o efeito em T2 predomina, reduzindo a intensidade do sinal. Os paramagnetos são atualmente os mais amplamente utilizados na prática diagnóstica clínica.
Agentes de contraste superparamagnéticos
O efeito dominante do óxidode ferro superparamagnético é o encurtamento do relaxamento T2. Com o aumento da dose, ocorre uma diminuição na intensidade do sinal. ACs ferromagnéticos, que incluem óxidos de ferro ferromagnéticos estruturalmente semelhantes à ferrita de magnetita (Fe2 + OFe23 + O3 ), também podem ser incluídos neste grupo de ACs.
A classificação a seguir é baseada na farmacocinética do CA (Sergeev PV et al., 1995):
- extracelular (não específico do tecido);
- gastrointestinal;
- organotrópico (específico do tecido);
- macromoleculares, que são usadas para determinar o espaço vascular.
Na Ucrânia, são conhecidos quatro MR-CA, que são CA paramagnéticos hidrossolúveis extracelulares, dos quais a gadodiamida e o ácido gadopentético são amplamente utilizados. Os demais grupos de CA (2-4) estão em ensaios clínicos no exterior.
MR-CA extracelular solúvel em água
Nome internacional |
Fórmula química |
Estrutura |
Ácido gadopentético |
Penta-acetato de gadolínio dimeglumina dietilenotriamina ((NMG)2Gd-DTPA) |
Linear, iônico |
Ácido gadotérico |
(NMG)Gd-DOTA |
Cíclico, iônico |
Gadodiamida |
Pentaacetato de dietilenotriamina de gadolínio-bis-metilamida (Gd-DTPA-BMA) |
Linear, não iônico |
Gadoteridol |
Gd-HP-D03A |
Cíclico, não iônico |
Os CA extracelulares são administrados por via intravenosa, 98% deles são excretados pelos rins, não penetram a barreira hematoencefálica, apresentam baixa toxicidade e pertencem ao grupo das substâncias paramagnéticas.
Contraindicações à ressonância magnética
Contraindicações absolutas incluem condições nas quais o exame representa uma ameaça à vida dos pacientes. Por exemplo, a presença de implantes ativados eletronicamente, magneticamente ou mecanicamente – principalmente marcapassos artificiais. A exposição à radiação de radiofrequência de um aparelho de ressonância magnética pode interromper o funcionamento de um marcapasso operando no sistema de solicitação, uma vez que alterações nos campos magnéticos podem imitar a atividade cardíaca. A atração magnética também pode fazer com que o marcapasso se mova em seu soquete e mova os eletrodos. Além disso, o campo magnético cria obstáculos à operação de implantes ferromagnéticos ou eletrônicos do ouvido médio. A presença de válvulas cardíacas artificiais é perigosa e constitui uma contraindicação absoluta apenas quando examinadas em aparelhos de ressonância magnética com campos altos e se houver suspeita clínica de dano à válvula. Contraindicações absolutas ao exame também incluem a presença de pequenos implantes cirúrgicos metálicos (clipes hemostáticos) no sistema nervoso central, uma vez que seu deslocamento devido à atração magnética ameaça sangramento. Sua presença em outras partes do corpo representa um risco menor, uma vez que, após o tratamento, a fibrose e o encapsulamento dos grampos ajudam a mantê-los estáveis. Entretanto, além do perigo potencial, a presença de implantes metálicos com propriedades magnéticas em qualquer caso causa artefatos que criam dificuldades na interpretação dos resultados do estudo.
Contraindicações à ressonância magnética
Absoluto: |
Parente: |
Marcapassos |
Outros estimulantes (bombas de insulina, estimuladores nervosos) |
Implantes de ouvido médio ferromagnéticos ou eletrônicos |
Implantes de ouvido interno não ferromagnéticos, próteses de válvula cardíaca (em campos altos, se houver suspeita de disfunção) |
Clipes hemostáticos de vasos cerebrais |
Clipes hemostáticos em outros locais, insuficiência cardíaca descompensada, gravidez, claustrofobia, necessidade de monitoramento fisiológico |
Contraindicações relativas, além das listadas acima, incluem insuficiência cardíaca descompensada, necessidade de monitorização fisiológica (ventilação mecânica, bombas de infusão elétricas). A claustrofobia é um obstáculo ao exame em 1 a 4% dos casos. Ela pode ser superada, por um lado, pelo uso de dispositivos com ímãs abertos, por outro, por uma explicação detalhada do dispositivo e do curso do exame. Não há evidências de efeitos nocivos da ressonância magnética sobre o embrião ou feto, mas recomenda-se evitar a ressonância magnética no primeiro trimestre da gravidez. O uso da ressonância magnética durante a gravidez é indicado nos casos em que outros métodos de diagnóstico por imagem não ionizantes não fornecem informações satisfatórias. O exame de ressonância magnética requer mais participação do paciente do que a tomografia computadorizada, uma vez que os movimentos do paciente durante o exame têm um efeito muito maior na qualidade das imagens, portanto, o exame de pacientes com patologia aguda, comprometimento da consciência, condições espásticas, demência, bem como crianças, costuma ser difícil.

