Médico especialista do artigo
Novas publicações
Papel das alterações do osso subcondral na patogénese da osteoartrite
Última revisão: 04.07.2025

Todo o conteúdo do iLive é medicamente revisado ou verificado pelos fatos para garantir o máximo de precisão factual possível.
Temos diretrizes rigorosas de fornecimento e vinculamos apenas sites de mídia respeitáveis, instituições de pesquisa acadêmica e, sempre que possível, estudos médicos revisados por pares. Observe que os números entre parênteses ([1], [2], etc.) são links clicáveis para esses estudos.
Se você achar que algum dos nossos conteúdos é impreciso, desatualizado ou questionável, selecione-o e pressione Ctrl + Enter.
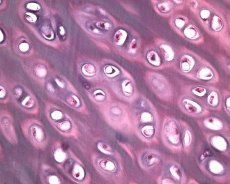
Juntamente com a degeneração da cartilagem articular, o tecido ósseo subjacente também está envolvido no processo patológico da osteoartrose. Supõe-se que o espessamento da placa subcondral contribua para a progressão da osteoartrose. À medida que a osteoartrose progride, a cartilagem articular, que está sujeita a estresse mecânico e químico, sofre erosão lenta devido a um desequilíbrio nos processos de catabolismo e reparação da cartilagem. Em particular, o estresse mecânico em relação às articulações que "suportam" o peso corporal contribui para a formação de um grande número de microfraturas na placa subcondral e na cartilagem. À medida que a cartilagem articular sofre erosão, a esclerose do osso subcondral progride e a rigidez do tecido ósseo aumenta, o que, por sua vez, contribui para uma maior ruptura da estrutura da cartilagem articular. No entanto, a questão da natureza primária ou secundária das alterações do osso subcondral na osteoartrose permanece sem solução.
Até recentemente, alterações radiograficamente detectáveis na substância esponjosa do osso subcondral, como esclerose ou formação de cistos, eram consideradas secundárias em pacientes com osteoartrose. No entanto, os resultados de estudos clínicos e experimentais indicam um possível papel inicial do osso subcondral na patogênese da osteoartrose. Um dos possíveis mecanismos é um aumento acentuado no gradiente de rigidez do osso subcondral devido ao fato de que a integridade do tecido cartilaginoso subjacente depende das propriedades mecânicas de seu "leito" ósseo. Estudos em primatas mostraram que alterações no osso subcondral podem preceder alterações na cartilagem articular. As evidências a favor e contra essa hipótese, que surgiram como resultado de estudos em modelos animais de osteoartrose e estudos clínicos, apenas intensificaram o debate. O espessamento das trabéculas no osso subcondral nem sempre é acompanhado por um aumento na mineralização óssea, ou melhor, um aumento no volume do osteoide. Este sinal de mineralização anormal indica que a perturbação da regulação da remodelação óssea é parte integrante da osteoartrite e também corrobora o conceito de defeito das células ósseas na osteoartrite. O grupo de J. Dequeker (1989) considera esta última uma "doença óssea metabólica generalizada".
O tecido ósseo é constantemente renovado. Este processo dinâmico, chamado remodelação óssea, é uma sequência complexa de reabsorção e mineralização. Os osteoclastos reabsorvem o tecido ósseo e os osteoblastos secretam proteínas que formam o principal componente orgânico para a mineralização. A formação e a reabsorção óssea não ocorrem aleatoriamente em todo o esqueleto; é um processo programado que ocorre em diferentes áreas do esqueleto, chamadas unidades de remodelação óssea. No início do ciclo, os osteoclastos aparecem na superfície inativa; dentro de 2 semanas, eles formam um túnel no osso cortical ou uma lacuna na superfície do osso trabecular. A frequência de ativação de novas unidades de remodelação óssea determina o grau de renovação óssea. Em uma pessoa jovem e saudável, os processos de formação e reabsorção óssea são equilibrados e a massa óssea normal é mantida. Na regulação hormonal da reabsorção do tecido ósseo, pelo menos PTH e PGE2 , não apenas os osteoclastos, mas também os osteoblastos participam, uma vez que sob a influência desses hormônios, fatores que estimulam a reabsorção óssea pelos osteoclastos são liberados. Atualmente, são conhecidos mais de 12 reguladores locais e sistêmicos do crescimento do tecido ósseo que afetam sua remodelação, em particular PTH, 1,25(OH) 2D3 ,calcitonina, hormônio do crescimento, glicocorticoides, hormônios tireoidianos, insulina, IGF (1 e 2), estrogênios, PGE2 , andrógenos.
As células ósseas liberam diversas proteínas e citocinas que realizam a regulação endócrina e a transdução de sinais. As proteínas produzidas pelos osteoblastos incluem proteínas da matriz óssea, como colágeno, osteopontina, osteocalcina e sialoproteínas ósseas. Além disso, essas células liberam proteases, tanto em suas formas ativas quanto latentes, que participam do processo de remodelação do tecido ósseo – MMPs, componentes do sistema ativador do plasminogênio (AP)/plasmina. As citocinas liberadas pelos osteoblastos podem atuar tanto por mecanismos autócrinos quanto por vias parácrinas em células locais (outros osteoblastos, osteoclastos).
Ainda não se sabe se esses sinais são regulados por estresse mecânico ou outros sinais químicos induzidos por estresse mecânico. No entanto, sabe-se que o estresse mecânico repetido causa proliferação local de células e/ou proteínas ósseas. In vivo, a carga mecânica pode ativar osteoblastos, aumentar o nível de nucleotídeos cíclicos, a produção de prostaglandinas e causar alterações morfológicas associadas à remodelação óssea. In vitro, o estresse mecânico causa proliferação de culturas de osteoblastos, expressão de mRNA de proteínas ósseas envolvidas na formação e mineralização de osteoides, liberação de fatores de crescimento locais, como IGF-1 e IGF-2, e moléculas de adesão. A transmissão do sinal de estresse mecânico pode ser realizada por meio de canais iônicos mecanossensíveis.
Há evidências indiretas de disfunção osteoblástica na osteoartrose. G. Gevers e J. Dequeker (1987) demonstraram um aumento nos níveis séricos de osteocalcina em mulheres com osteoartrose da mão, bem como em explantes de osso cortical, indicando que a patologia óssea pode ser parte da osteoartrose. A autópsia revelou não apenas espessamento do osso subcondral, mas também mineralização anormalmente baixa da cabeça femoral. Em cobaias com osteoartrose induzida cirurgicamente, a tomografia computadorizada revelou espessamento significativo da fração óssea na zona subcondral. Um desequilíbrio entre proteínas colágenas e não colágenas (osteocalcina, etc.) pode levar a um aumento no volume ósseo, mas não afeta sua densidade mineral. De acordo com M. Shimizu et al. (1993), a progressão das alterações degenerativas na cartilagem articular está associada a uma remodelação mais intensiva do osso subcondral e a um aumento em sua rigidez, o que também indica um defeito nas células do tecido ósseo na osteoartrose. Segundo a hipótese proposta por B. Lee e M. Aspden (1997), a proliferação de células ósseas defeituosas pode levar ao aumento da rigidez do tecido ósseo, mas não causa aumento da sua densidade mineral.
CI Westacott et al. (1997) levantaram a hipótese de que osteoblastos anormais afetam diretamente o metabolismo da cartilagem. Cultivando osteoblastos de pacientes com osteoartrite com condrócitos de pessoas sem doenças articulares, os autores observaram uma alteração significativa na liberação de glicosaminoglicanos pelo tecido cartilaginoso normal in vitro, mas o nível de liberação de citocinas permaneceu inalterado. G. Hilal et al. (1998) demonstraram que a cultura de osteoblastos do osso subcondral de pacientes com osteoartrite in vitro apresenta um metabolismo alterado — a atividade do sistema AP/plasmina e o nível de IGF-1 nessas células estão aumentados. A observação de CI Westacott et al. (1997) pode ser explicada por um aumento na atividade de proteases em células ósseas subcondrais.
Ainda não se sabe se alterações no osso subcondral iniciam a osteoartrite ou contribuem para sua progressão. DK Dedrick et al. (1993) demonstraram que, em cães com osteoartrite induzida cirurgicamente, o espessamento do osso subcondral não é uma condição necessária para o desenvolvimento de alterações semelhantes à osteoartrose na cartilagem articular, mas contribui para a progressão de processos degenerativos na cartilagem. Os resultados do estudo de A. Sa'ied et al. (1997) contradizem os dados do estudo anterior. Usando ecografia de 50 MHz para avaliar as alterações morfológicas iniciais e sua progressão na cartilagem articular e no osso na osteoartrite experimental induzida por injeções de ácido monoiodoacético na articulação do joelho de ratos, os autores demonstraram um processo simultâneo de alterações no osso e na cartilagem durante os três primeiros dias após a injeção.
Os osteoblastos secretam fatores de crescimento e citocinas envolvidos na remodelação óssea local, que podem promover a remodelação da cartilagem adequada em articulações que suportam peso após sua penetração através de microfissuras na camada calcificada da cartilagem articular. Além disso, produtos secretórios de células ósseas são encontrados no líquido sinovial. Os produtos mais prováveis secretados por osteoblastos anormais que podem iniciar o processo de remodelação da cartilagem local são o TGF-β e as proteínas morfométricas ósseas (BMPs). Ambos os membros da família TGF são secretados por condrócitos e osteoblastos, e ambos são capazes de modificar a remodelação óssea e da cartilagem. J. Martel Pelletier et al. (1997) observaram um aumento no nível de TGF-β em explantes ósseos subcondrais de pacientes com osteoartrose em comparação com indivíduos saudáveis, o que indica um provável papel desse fator de crescimento na patogênese da osteoartrose. IGFs também são produzidos por osteoblastos. Em uma cultura de células semelhantes a osteoblastos obtidas de pacientes com osteoartrose, foi encontrado um aumento no nível de IGFs, que alteram o metabolismo da cartilagem.
TGF-β, IGF, BMP e citocinas produzidas por osteoblastos no osso subcondral podem influenciar a produção de colagenase e outras enzimas proteolíticas na cartilagem, o que, por sua vez, pode promover a remodelação/degradação da matriz cartilaginosa. Ainda não está claro se os osteoblastos na osteoartrite produzem menos fator estimulador de colônias de macrófagos (M-CSF – um estimulador da reabsorção óssea) do que as células normais. Os resultados dos estudos de AG Uitterlinden et al. (1997) mostraram que os receptores de vitamina D, expressos pelos osteoblastos e que regulam a expressão de diversos fatores sintetizados por essas células, podem desempenhar um papel na formação de osteófitos, o que explica parcialmente o papel dos osteoblastos na patogênese dessa doença.
Levando em consideração os resultados dos estudos acima, G. Hilal et al. (1998), J. Martel-Pelletier et al. (1997) propuseram a seguinte hipótese de trabalho sobre a relação entre a remodelação óssea subcondral e a cartilagem articular adequada na osteoartrose. Em um estágio inicial ou avançado da patogênese da OA, o processo de remodelação do tecido ósseo no osso subcondral se intensifica. Ao mesmo tempo, a carga repetida leva a microfraturas locais e/ou ao surgimento de um desequilíbrio no sistema IGF/proteína de ligação ao IGF (IGFBP) devido a uma resposta anormal dos osteoblastos do osso subcondral, o que contribui para sua esclerose. Esta última, por sua vez, pode contribuir para o surgimento de microfraturas da cartilagem adequada e danos à sua matriz.
Em condições normais, esse dano é reparado pela síntese e liberação local de IGF-1 e da proteína de ligação ao IGF, que estimulam a formação da MEC da cartilagem articular. Ao mesmo tempo, o sistema GF promove o crescimento de células ósseas subcondrais e a formação da matriz óssea. A atividade anabólica do sistema IGF é aumentada no osso subcondral de pacientes com osteoartrose, enquanto a ativação local do sistema AP/plasmina (um regulador local do sistema IGF) na cartilagem articular causa suas alterações locais. Em osteoblastos com osteoartrose, o IGF-1 interrompe a regulação do AP pela plasmina pelo tipo de feedback positivo, portanto, pode restringir a remodelação no tecido ósseo, o que, em última análise, leva à esclerose subcondral. Assim, no tecido ósseo e cartilaginoso, a indução local de IGF-1 e proteases leva, por um lado, ao dano da cartilagem e, por outro, ao espessamento do osso subcondral, este último, por sua vez, contribuindo para maiores danos à cartilagem. O desequilíbrio entre o dano à cartilagem associado à esclerose subcondral e sua capacidade reparadora leva a alterações progressivas na matriz extracelular da cartilagem e ao desenvolvimento de osteoartrose. Segundo os autores, essa hipótese também explica a lenta progressão da doença.

