Médico especialista do artigo
Novas publicações
Diagnóstico das fases do curso do cancro da próstata
Última revisão: 04.07.2025

Todo o conteúdo do iLive é medicamente revisado ou verificado pelos fatos para garantir o máximo de precisão factual possível.
Temos diretrizes rigorosas de fornecimento e vinculamos apenas sites de mídia respeitáveis, instituições de pesquisa acadêmica e, sempre que possível, estudos médicos revisados por pares. Observe que os números entre parênteses ([1], [2], etc.) são links clicáveis para esses estudos.
Se você achar que algum dos nossos conteúdos é impreciso, desatualizado ou questionável, selecione-o e pressione Ctrl + Enter.
Clinicamente, é feita uma distinção entre câncer localizado (T 1-2, N 0, M 0 ), localmente avançado (T 3-4, N 0-1, M 0 ) e generalizado (T 1-4, N 0-1, M 1 ).
Pacientes com estágios clinicamente localizados e localmente avançados são classificados de acordo com o grau de risco (D'Amico A V. et al., 2003):
- baixo: estágio T 1a-c; nível de PSA menor que 10 ig/ml: classificação de Gleason - 2-5; na biópsia - lesão unilateral menor que 50%:
- moderado: estágio T 2a; nível de PSA menor que 10 ng/ml; escore de Gleason - 3 + 4 = 7; na biópsia - lesão bilateral menor que 50%;
- estágio alto T 2b, T 3a-b; nível de PSA - 10-20 ng/ml; classificação de Gleason - mais de 4 + 3 - 7; na biópsia - dano maior que 50%, invasão perineural;
- muito alto: estágio T 4; nível de PSA acima de 20 ng/ml; pontuação de Gleason acima de 8; biópsia mostra invasão linfovascular.
Após o diagnóstico ser esclarecido e a extensão do processo ser estabelecida (localizada, localmente avançada ou generalizada), o médico e o paciente se deparam com a escolha do método de tratamento. Na sociedade moderna, atribui-se grande importância à qualidade de vida dos pacientes após o início do tratamento. A qualidade de vida sem tratamento corresponde ao curso da doença de base e depende da progressão do processo oncológico. As mudanças na qualidade de vida ocorrem principalmente após o início do tratamento e a utilização de um dos métodos terapêuticos ou cirúrgicos. Estabelecer claramente o estágio do processo permite não apenas escolher o método de tratamento ideal, mas também prever o curso posterior da doença.
A determinação do nível de PSA em combinação com o quadro clínico do câncer de próstata e a gradação do tumor pela escala de Gleason aumenta significativamente o conteúdo informativo de cada um dos indicadores listados no estabelecimento do estadiamento patológico do câncer. AV Partin et al. (1997) propuseram tabelas prognósticas que permitem prever a disseminação do tumor, a escolha do método de tratamento, o grau de radicalidade e o prognóstico da eficácia do tratamento.
Para avaliar a disseminação do tumor, os métodos mais comumente utilizados são o toque retal, o ultra-som transesofágico (USTR), a dosagem do PSA e a cintilografia óssea. Se necessário, são prescritas tomografia computadorizada (TC) ou ressonância magnética (RM) e radiografia de tórax.
Qualquer um dos métodos de imagem é projetado para determinar o estágio e avaliar a eficácia do tratamento. Após a confirmação do diagnóstico, o urologista deve esclarecer o volume do tumor primário, seus limites e o potencial invasivo ou metastático do tumor. Todos esses indicadores são de grande importância para o prognóstico da doença e a escolha do método de tratamento.
Tumor primário (T)
Primeiramente, é necessário determinar se o tumor está limitado à próstata (T 1-2 ) ou se estende além da cápsula (T 3-4 ). O exame digital frequentemente não permite avaliar a extensão do tumor. Segundo alguns dados, os resultados do toque retal correspondem aos do exame histológico em menos de 50% dos pacientes. No entanto, um exame mais detalhado é indicado apenas na decisão por um tratamento radical.
O nível de PSA pode refletir a extensão do tumor, mas não permite uma determinação precisa do estágio morfológico. A combinação do nível de PSA, do índice de Gleason e dos dados de palpação permite uma melhor previsão do estágio morfológico do que cada um desses parâmetros separadamente. O valor do PSA livre é controverso: em um estudo, a determinação do conteúdo de PSA livre ajudou a esclarecer o estágio em tumores localizados, mas outros estudos não confirmaram isso. Somente estudos aprofundados ajudarão a resolver essa questão.
A ultrassonografia transretal é mais frequentemente usada para examinar a condição da próstata. Este método pode detectar apenas 60% dos tumores e nem sempre mostra invasão capsular. Quase 60% dos pacientes com estágio T3 . A ultrassonografia indica um processo menos comum. Os sinais ultrassonográficos de invasão capsular são protuberância, irregularidade e ruptura do contorno da glândula. A invasão de células tumorais nas vesículas seminais é um sinal de mau prognóstico, mas informações sobre isso são extremamente importantes para a escolha de um método de tratamento. Ao realizar TRUS, deve-se prestar atenção à ecoestrutura das vesículas (hiperecogenicidade), sua assimetria, deformação e expansão. Além disso, o dano às vesículas seminais é indicado pela perda de redondeza e compactação na base da glândula. Esses sinais são bastante subjetivos, portanto, é inadequado confiar inteiramente nos dados do ultrassom. A invasão das vesículas seminais indica um alto risco de recidiva local e metástases, e sua biópsia é indicada para esclarecimento (antes da cirurgia). O exame não deve ser iniciado com este procedimento, mas se o risco de invasão for alto e a escolha do tratamento depender do resultado da biópsia, sua implementação é justificada. Um resultado negativo não exclui a invasão microscópica. Como regra, uma biópsia das vesículas seminais é realizada no estádio clínico T 2b e superior e o conteúdo de PSA é superior a 10 ng/ml. O resultado é considerado positivo se pelo menos uma biópsia da base da próstata contiver células tumorais. Não apenas estudos adicionais, mas também uma análise completa dos resultados da biópsia primária permitem aumentar a precisão da determinação clínica do estádio (o número e a extensão dos focos tumorais e a invasão capsular desempenham um papel). O grau de diferenciação também é importante: com um índice de Gleason inferior a 6, o tumor é localizado em 70% dos casos.
O fluxo sanguíneo na próstata com câncer é maior do que em uma glândula normal ou com hiperplasia. Após a castração, a intensidade do fluxo sanguíneo na glândula diminui. O desenvolvimento de mapas ecodopplerográficos para o diagnóstico e monitoramento do câncer de próstata é promissor, mas atualmente não há dados confiáveis sobre o uso da ecodopplerografia na determinação do estágio do processo local. É possível usar esse método para obter material adicional durante biópsia direcionada de focos de vascularização patológica.
Os resultados da visualização do câncer de próstata dependem diretamente do equipamento técnico da clínica e da experiência do especialista. É por isso que todos os métodos modernos de visualização desempenham um papel não determinante, mas esclarecedor, e a escolha do método de tratamento se baseia na combinação de dados de exames clínicos e estudos instrumentais.
A ressonância magnética possui os melhores recursos para visualizar a estrutura da próstata. O padrão moderno para examinar os órgãos pélvicos usando o método de ressonância magnética é o uso de um sensor endorretal, que permite obter uma imagem com a maior resolução espacial possível de 0,5-1 mm. Forçar o ar para dentro do sensor endorretal proporciona uma visualização clara da cápsula da próstata, ângulos retoprostáticos e fáscia retoprostática de Denonvilliers. O uso de um sensor endorretal na ressonância magnética não limita a visualização dos linfonodos regionais (até o nível da bifurcação da aorta abdominal). O câncer de próstata é caracterizado por baixa intensidade de sinal em imagens ponderadas em T contra o fundo de um sinal de alta intensidade de uma zona periférica inalterada da glândula. Forma irregular, disseminação difusa com efeito de massa, contornos difusos e irregulares são características morfológicas de focos de baixa intensidade de sinal na zona periférica da próstata, sugerindo uma natureza neoplásica da lesão. Ao realizar o contraste dinâmico, os focos cancerosos acumulam rapidamente o agente de contraste na fase arterial e o removem rapidamente, o que reflete o grau de angiogênese e, consequentemente, o grau de malignidade do tumor. A baixa intensidade de sinal também é característica de focos de hemorragias pós-biópsia, prostatite, hiperplasia benigna estromal da zona neutra da glândula, alterações fibrocicatriciais, hiperplasia fibromuscular e consequências de terapia hormonal ou radioterapia. A RM sem contraste dinâmico não permite a diferenciação confiável da maioria das alterações e doenças listadas.
Como observado acima, uma das principais tarefas de qualquer método de imagem para câncer de próstata é determinar o volume da lesão da glândula e a disseminação do tumor além da cápsula. A determinação do volume do tumor é importante para o prognóstico. Um volume tumoral inferior a 4 cm³ indica metástases à distância, e 12 cm³ indica uma probabilidade extremamente alta de metástases. De acordo com pesquisas, a precisão da ressonância magnética na detecção de focos de lesões neoplásicas da próstata varia de 50 a 90%. A sensibilidade da ressonância magnética na determinação da localização do câncer de próstata é de cerca de 70-80%, enquanto focos microscópicos de câncer (focos) não podem ser detectados por meio da ressonância magnética.
A vantagem mais importante da ressonância magnética endorretal é a capacidade de localizar lesões neoplásicas em áreas inacessíveis a outros métodos diagnósticos e de esclarecer a natureza e a direção do crescimento tumoral. Por exemplo, a ressonância magnética permite a detecção de lesões neoplásicas nas partes anteriores da zona periférica da próstata, inacessíveis à biópsia transretal. Em geral, a ressonância magnética complementa significativamente os dados do toque retal e do ultrassom transretal (USTR) sobre a localização tumoral.
A ressonância magnética endorretal permite a visualização da cápsula glandular, feixes vasculonervosos, vesículas seminais, ápice glandular, plexo venoso periprostático e determinação da prevalência local de tumor glandular. Deve-se enfatizar que a penetração da cápsula é considerada um sinal microscópico, e mesmo os aparelhos de ressonância magnética modernos (bobina endorretal) não são capazes de fornecer tal informação. Só é possível obter dados sobre o crescimento além da cápsula glandular.
Critérios diagnósticos para extensão extracapsular usando ressonância magnética:
- a presença de um tumor extracapsular;
- contorno irregular da glândula (deformação, angularidade);
- assimetria dos feixes neurovasculares;
- obliteração dos ângulos retoprostáticos;
- amplo contato do tumor com a cápsula.
A maior especificidade (até 95-98%) e acurácia dos resultados de ressonância magnética são alcançadas ao examinar pacientes com risco médio ou alto de invasão extracapsular. Acredita-se que a invasão extracapsular (de acordo com dados de ressonância magnética) indique a inadequação do tratamento cirúrgico e um prognóstico desfavorável para a doença. A terapia hormonal ou radioterapia não afeta a precisão da detecção da disseminação extracapsular do tumor de próstata. A principal dificuldade na detecção de focos de câncer e disseminação extracapsular do tumor é a alta variabilidade da interpretação do tomógrafo por diferentes especialistas. A principal tarefa de um especialista em radiodiagnóstico é alcançar alta especificidade diagnóstica (mesmo à custa da sensibilidade) para não privar pacientes operáveis da chance de tratamento radical.
A similaridade da densidade do tecido prostático canceroso, hiperplásico e normal na TC torna este método pouco útil para avaliar a disseminação local do tumor. A invasão das vesículas seminais é mais importante do que a invasão das cápsulas, mas mesmo neste caso a TC fornece informações apenas em casos avançados. No entanto, este método é usado ativamente para marcar a área de impacto antes da radioterapia.
O lento desenvolvimento do diagnóstico por radiação em nosso país levou ao diagnóstico tardio do câncer de próstata e, consequentemente, à prevalência insuficiente de métodos radicais de tratamento do câncer de próstata (por exemplo, prostatectomia), à baixa disponibilidade de tomógrafos modernos e à ausência de programas de treinamento adequados para especialistas em diagnóstico por radiação e urologistas. Apesar da ampla difusão da tomografia computadorizada e da ressonância magnética, o nível de equipamentos dos consultórios e a formação de especialistas em diagnóstico por radiação são insuficientes para que as informações obtidas sejam decisivas na escolha de um método de tratamento para pacientes com câncer de próstata.
Linfonodos regionais (N)
Os linfonodos regionais devem ser avaliados apenas quando isso afetar diretamente a estratégia de tratamento (geralmente no planejamento de um tratamento radical). Níveis elevados de PSA, tumores T2c -T3a, baixa diferenciação e invasão perineural estão associados a um alto risco de metástase linfonodal. A avaliação do estado dos linfonodos com base nos níveis de PSA é considerada insuficiente.
Somente a linfadenectomia (aberta ou laparoscópica) fornece as informações necessárias. Estudos recentes de linfadenectomia estendida demonstraram que o câncer de próstata nem sempre afeta os linfonodos obturadores. Em tumores assintomáticos e níveis de PSA inferiores a 20 kg/ml, a TC confirma linfonodos aumentados em apenas 1% dos casos. O uso de RM ou TC é justificado em casos de alto risco de metástase, pois a especificidade desses métodos atinge 93-96%. No entanto, mesmo um resultado positivo ao utilizá-los pode ser falso, e somente a punção de um linfonodo suspeito permite recusar a linfadenectomia. De acordo com a análise retrospectiva, o tamanho do linfonodo nem sempre indica a presença de metástases; a assimetria dos linfonodos afetados é considerada um sinal mais informativo. Atualmente, apenas 2-3% dos pacientes submetidos à prostatectomia radical para câncer de próstata localizado são diagnosticados com metástase para os linfonodos com base no exame histológico pós-operatório.
A tomografia por emissão de pósitrons (PET) e a cintilografia com anticorpos marcados são recomendadas como métodos para detecção de metástases em linfonodos, mas seu uso ainda é limitado devido à sensibilidade insuficiente.
Os nomogramas de Partin (2001) podem ser usados para avaliar o risco de envolvimento de linfonodos regionais. Os nomogramas são algoritmos matemáticos usados para um paciente específico ou um grupo de pacientes. Essas tabelas permitem determinar a probabilidade de disseminação local do tumor (para a cápsula, vesículas seminais) e envolvimento de linfonodos com base no estágio clínico, nível de PSA e índice de Gleason. Em particular, elas permitem identificar um grupo de pacientes com baixa probabilidade (menos de 10%) de metástase de linfonodos (com nível de PSA acima de 20 ng/m2, estágio T 1-2a e índice de Gleason 2-6); nesse grupo, a condição dos linfonodos pode não ser especificada antes do tratamento radical. O risco de metástase de linfonodos também pode ser avaliado pela detecção de áreas tumorais com anaplasia pronunciada (4-5 pontos): se tais áreas forem encontradas em quatro ou mais biópsias ou se predominarem em pelo menos uma biópsia, o risco chega a 20-45%. Em outros pacientes, não excede 2,5%. Exames adicionais não são necessários nesses casos.
Metástases à distância (M)
Em 85% dos pacientes que morrem de câncer de próstata, são detectadas lesões do esqueleto axial. Metástases ósseas ocorrem devido à penetração de células cancerígenas na medula óssea com a corrente sanguínea, o que leva ao crescimento tumoral e à lise das estruturas ósseas. A prevalência de metástases ósseas afeta o prognóstico, e sua detecção precoce alerta o médico sobre possíveis complicações. Em 70% dos casos, a metástase é combinada com um aumento na atividade da isoenzima óssea da fosfatase alcalina (FAL). A determinação da atividade da FAL e do nível de PSA na grande maioria dos casos nos permite detectar metástases ósseas. De acordo com a análise multivariada, esses indicadores são afetados apenas pelo número de metástases ósseas. É importante que a atividade da isoenzima óssea FAL reflita o grau de dano ósseo com mais precisão do que o nível de PSA.
A cintilografia é considerada o método mais sensível para a detecção de metástases ósseas (é superior à radiografia e à determinação da atividade das fosfatases alcalina e ácida). Os difosfonatos de tecnécio são mais bem utilizados como radiofármacos, visto que sua acumulação nos ossos é muito mais ativa do que nos tecidos moles. Foi demonstrada uma correlação entre a avaliação semiquantitativa do dano ósseo e a sobrevida. A detecção de metástases à distância é possível em qualquer órgão. Elas ocorrem mais frequentemente em linfonodos não regionais, pulmões, fígado, cérebro e pele. Em caso de queixas e sintomas correspondentes, radiografia de tórax, ultrassonografia, tomografia computadorizada e ressonância magnética são utilizadas para detectá-las. As táticas para suspeita de metástase óssea são apresentadas no diagrama.
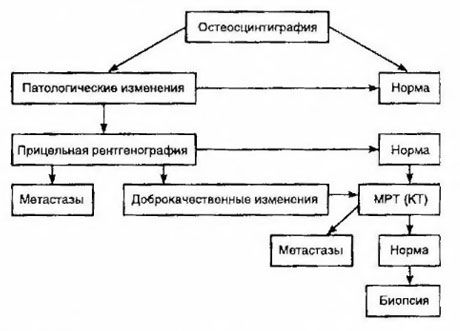
O indicador laboratorial mais confiável para determinar o grau de metástase é o nível de PSA. Foi demonstrado que um aumento acima de 100 ng/ml é o único parâmetro que indica com segurança metástases à distância. A determinação do nível de PSA reduz o número de pacientes que necessitam de cintilografia óssea. A probabilidade de detectar metástases ósseas com uma diminuição no nível de PSA é muito baixa. Na ausência de queixas e com um nível inicial de PSA inferior a 20 ng/ml, a cintilografia pode ser evitada na detecção de tumores altamente e moderadamente diferenciados. Ao mesmo tempo, no caso de tumores pouco diferenciados e invasão capsular, a cintilografia é indicada (independentemente do nível de PSA).


 [
[