Novas publicações
Novos mecanismos genéticos podem ser um alvo terapêutico contra o glioma
Última revisão: 02.07.2025

Todo o conteúdo do iLive é medicamente revisado ou verificado pelos fatos para garantir o máximo de precisão factual possível.
Temos diretrizes rigorosas de fornecimento e vinculamos apenas sites de mídia respeitáveis, instituições de pesquisa acadêmica e, sempre que possível, estudos médicos revisados por pares. Observe que os números entre parênteses ([1], [2], etc.) são links clicáveis para esses estudos.
Se você achar que algum dos nossos conteúdos é impreciso, desatualizado ou questionável, selecione-o e pressione Ctrl + Enter.
Um estudo do laboratório de Shi-Yuan Cheng, PhD, professor da Divisão Ken e Ruth Davey de Neuro-Oncologia do Departamento de Neurologia, identificou novos mecanismos subjacentes a eventos alternativos de splicing de RNA em células tumorais de glioma que podem servir como novos alvos terapêuticos. Os resultados do estudo foram publicados no periódico Journal of Clinical Investigation.
"Descobrimos uma maneira diferente de tratar o glioma através da lente do splicing alternativo e descobrimos novos alvos que não foram identificados anteriormente, mas são importantes para a malignidade do glioma", disse Xiao Song, MD, PhD, professor associado de neurologia e principal autor do estudo.
Gliomas são o tipo mais comum de tumor cerebral primário em adultos e se originam de células gliais, que residem no sistema nervoso central e dão suporte aos neurônios vizinhos. Gliomas são altamente resistentes aos tratamentos convencionais, incluindo radiação e quimioterapia, devido à heterogeneidade genética e epigenética do tumor, o que reforça a necessidade de encontrar novos alvos terapêuticos.
Pesquisas anteriores do laboratório Cheng, publicadas no periódico Cancer Research, mostraram que o importante fator de splicing SRSF3 é significativamente elevado em gliomas em comparação com cérebros normais, e o splicing de RNA regulado por SRSF3 promove o crescimento e a progressão do glioma ao influenciar múltiplos processos celulares em células tumorais.
O splicing de RNA é um processo que envolve a remoção de íntrons (regiões não codificantes do RNA) e a união de éxons (regiões codificantes) para formar uma molécula de mRNA madura que dá suporte à expressão genética em uma célula.
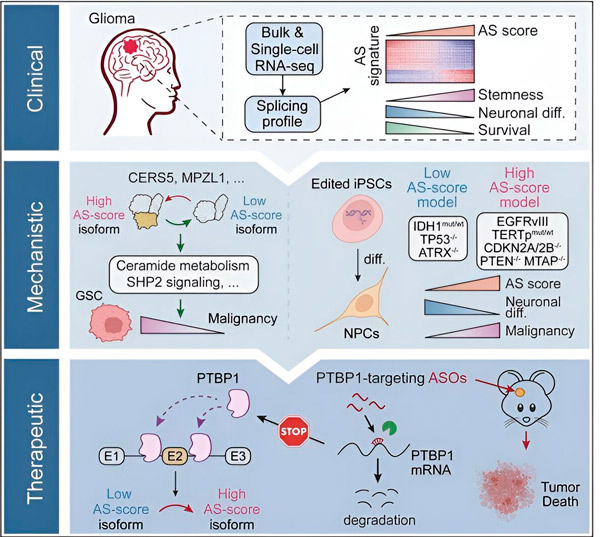
No presente estudo, os cientistas tiveram como objetivo identificar alterações no splicing alternativo em células tumorais de glioma, os mecanismos subjacentes a essas alterações e determinar seu potencial como alvos terapêuticos.
Utilizando métodos computacionais e tecnologias de sequenciamento de RNA, os pesquisadores examinaram alterações de splicing em células tumorais de glioma de amostras de pacientes. Para confirmar essas alterações, eles utilizaram tecnologias de edição genética CRISPR para introduzir diferentes mutações de driver de glioma em modelos de glioma derivados de células-tronco pluripotentes induzidas (iPSCs) humanas.
Eles descobriram que essas alterações de splicing são intensificadas por uma variante do receptor do fator de crescimento epidérmico III (EGFRIII), que é conhecido por ser superexpresso em muitos tumores, incluindo gliomas, e é inibido por uma mutação no gene IDH1.
Pesquisadores confirmaram a função de dois eventos de splicing de RNA que criam diferentes isoformas de proteínas com diferentes sequências de aminoácidos.
"Apenas uma dessas isoformas pode promover o crescimento tumoral, ao contrário da outra isoforma, que normalmente é expressa no cérebro normal. Os tumores exploram esse mecanismo para expressar seletivamente a isoforma promotora do tumor em detrimento da isoforma cerebral normal", disse Song.
Em seguida, a equipe analisou proteínas de ligação a RNA upstream e descobriu que o gene PTBP1 regula o splicing do RNA promotor de tumores em células de glioma. Utilizando um modelo de glioma ortotópico em camundongos imunodeficientes, os pesquisadores direcionaram a PTBP1 com terapia baseada em oligonucleotídeos antisense (ASO), que, por fim, suprimiu o crescimento tumoral.
"Nossos dados destacam o papel do splicing alternativo de RNA na influência da malignidade e heterogeneidade do glioma e seu potencial como uma vulnerabilidade terapêutica para o tratamento de gliomas adultos", escreveram os autores do estudo.
O próximo passo dos pesquisadores é explorar o potencial de direcionar o PTBP1 para provocar uma resposta imune antitumoral, disse Song.
"Usando a análise de sequenciamento de RNA de leitura longa, descobrimos que o direcionamento de PTBP1 em células de glioma resulta na produção de múltiplos transcritos com splicing alternativo que estão ausentes em tecidos normais. Portanto, nosso próximo projeto é descobrir se essa isoforma pode gerar alguns antígenos para que o sistema imunológico possa reconhecer melhor o tumor", disse Song.
Song também acrescentou que sua equipe está interessada em analisar alterações de splicing em células não tumorais de pacientes com glioma, como células imunes.
Já sabemos que o splicing é muito importante para regular a função na célula, portanto, ele não deve apenas regular a malignidade do tumor, mas também pode regular a função das células imunes para determinar se elas podem efetivamente matar o câncer. Por isso, também estamos realizando algumas análises de bioinformática em células imunes infiltradas por tumores para verificar se há alguma alteração no splicing após uma célula imune ter se infiltrado no tumor.
"Nosso objetivo é determinar o papel do splicing alternativo na formação do microambiente tumoral imunossupressor e identificar alvos potenciais para melhorar a eficácia das imunoterapias no glioma", disse Song.
