Novas publicações
Derivados de compostos de talidomida conduzem à morte de células cancerígenas resistentes
Última revisão: 02.07.2025

Todo o conteúdo do iLive é medicamente revisado ou verificado pelos fatos para garantir o máximo de precisão factual possível.
Temos diretrizes rigorosas de fornecimento e vinculamos apenas sites de mídia respeitáveis, instituições de pesquisa acadêmica e, sempre que possível, estudos médicos revisados por pares. Observe que os números entre parênteses ([1], [2], etc.) são links clicáveis para esses estudos.
Se você achar que algum dos nossos conteúdos é impreciso, desatualizado ou questionável, selecione-o e pressione Ctrl + Enter.
Um estudo conduzido pela Universidade Goethe, em Frankfurt, aponta para a possibilidade de que derivados da talidomida possam ser usados para tratar o câncer. A talidomida era vendida como pílula para dormir na década de 1950. Mais tarde, tornou-se notória por causar graves defeitos congênitos nos primeiros estágios da gravidez.
A molécula também é conhecida por marcar proteínas na célula para destruição. Como parte do estudo atual, cientistas criaram derivados da talidomida. Eles conseguiram demonstrar que essas substâncias afetam a destruição de proteínas responsáveis pela sobrevivência das células cancerígenas.
Talvez nenhuma outra molécula tenha tido um passado tão turbulento quanto a talidomida. Ela foi o ingrediente principal de um medicamento aprovado em muitos países na década de 1950 como sedativo e sonífero. Mas logo ficou claro que mulheres grávidas que tomavam talidomida frequentemente davam à luz bebês com deformidades graves.
No entanto, nas últimas décadas, a medicina voltou a depositar grandes esperanças nele. Estudos demonstraram, entre outras coisas, que ele inibe o crescimento dos vasos sanguíneos e, portanto, é potencialmente adequado para isolar tumores de seu meio nutriente. Posteriormente, também se mostrou muito eficaz no tratamento do mieloma múltiplo, um tumor maligno da medula óssea.
"Agora sabemos que a talidomida pode ser chamada de 'cola molecular'", explica o Dr. Xinglai Cheng, do Instituto de Química Farmacêutica da Universidade Goethe, em Frankfurt. "Isso significa que ela é capaz de agarrar duas proteínas e uni-las."
Isso é particularmente interessante porque uma dessas proteínas é uma espécie de "máquina de rotulagem": ela atribui um rótulo inequívoco de "LIXO" a outra proteína.
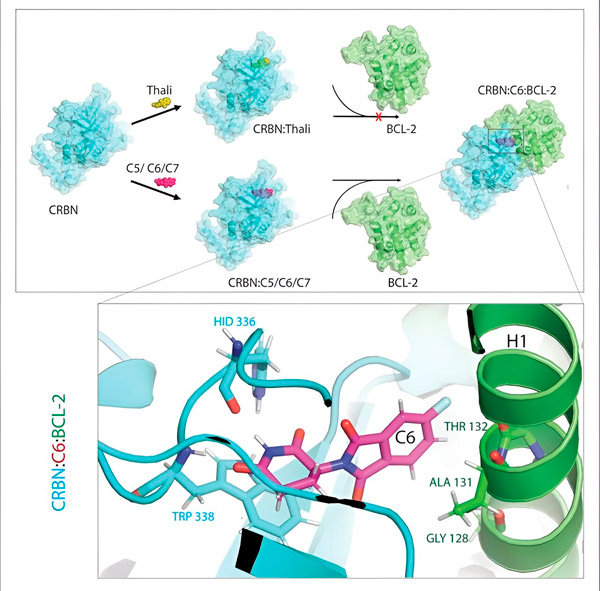
Os derivados da talidomida C5, C6 e C7 alteram o CRBN, a "máquina de marcação", para que ele possa se ligar ao BCL-2. Dessa forma, a molécula BCL-2 é marcada para degradação — uma possível nova estratégia para combater o câncer. Autor: Dr. Xinglai Cheng.
O sistema de eliminação de resíduos da célula reconhece essa marcação: ele captura a molécula de proteína marcada e a fragmenta. "Esse mecanismo explica os diferentes efeitos da talidomida", diz Cheng. "Dependendo da proteína marcada, ela pode causar deformidades durante o desenvolvimento embrionário ou destruir células malignas."
Esse mecanismo abre grandes possibilidades para a medicina, visto que as células cancerígenas dependem de certas proteínas para sobreviver. Se elas pudessem ser sistematicamente atacadas e destruídas, talvez a doença pudesse ser curada. O problema é que a cola molecular é bastante peculiar.
Um de seus parceiros de ligação é sempre a máquina de marcação da célula ou, em linguagem científica, uma ligase E3 chamada CRBN. Apenas algumas das milhares de proteínas no corpo podem ser o segundo parceiro — a escolha depende da cola.
"Então, criamos uma série de derivados da talidomida", diz Cheng. "Em seguida, testamos se eles tinham propriedades adesivas e, em caso afirmativo, contra quais proteínas eram eficazes." Para isso, os pesquisadores adicionaram seus derivados a todas as proteínas da linhagem celular cultivada. Em seguida, observaram quais dessas proteínas eram degradadas na presença de CRBN.
"No processo, identificamos três derivados que poderiam marcar uma proteína celular muito importante para a degradação, a BCL-2", explica Cheng. "A BCL-2 impede que as células ativem seu programa de autodestruição; portanto, se ela não estiver presente, as células morrem."
É por isso que o BCL-2 tem sido foco de pesquisas sobre o câncer há muito tempo. Existe até um medicamento para leucemia chamado Venetoclax que reduz a eficácia do BCL-2 e, portanto, causa a autodestruição das células mutadas.
"No entanto, em muitas células cancerígenas, a própria BCL-2 sofre mutação. Como resultado, o venetoclax não inibe mais a proteína", diz Cheng. "Conseguimos demonstrar que nossos derivados também sinalizam essa forma mutada para degradação. Além disso, nossos parceiros do Instituto Max Planck de Biofísica simularam a interação de derivados da talidomida com a BCL-2 em um computador. Isso mostrou que os derivados se ligam a sítios completamente diferentes dos do venetoclax — um resultado que posteriormente pudemos confirmar experimentalmente."
Os pesquisadores também testaram seus compostos em moscas-das-frutas com células cancerígenas. A taxa de sobrevivência das moscas tratadas dessa forma foi significativamente maior. No entanto, Cheng alerta para não criar muitas expectativas, pois esses resultados ainda são pesquisa básica. "Embora mostrem que as moléculas modificadas de talidomida têm grande potencial terapêutico, ainda não podemos afirmar se elas se comprovarão na prática em algum momento."
Os resultados do estudo foram publicados na revista Cell Reports Physical Science.
