Novas publicações
Sistema de administração de medicamentos em circuito fechado pode melhorar a administração de quimioterapia
Última revisão: 02.07.2025

Todo o conteúdo do iLive é medicamente revisado ou verificado pelos fatos para garantir o máximo de precisão factual possível.
Temos diretrizes rigorosas de fornecimento e vinculamos apenas sites de mídia respeitáveis, instituições de pesquisa acadêmica e, sempre que possível, estudos médicos revisados por pares. Observe que os números entre parênteses ([1], [2], etc.) são links clicáveis para esses estudos.
Se você achar que algum dos nossos conteúdos é impreciso, desatualizado ou questionável, selecione-o e pressione Ctrl + Enter.
Quando pacientes com câncer são submetidos à quimioterapia, as doses da maioria dos medicamentos são calculadas com base na área de superfície corporal do paciente. Essa estimativa é feita por meio de uma equação que leva em consideração a altura e o peso do paciente. Essa equação foi formulada em 1916 com base em dados de apenas nove pacientes.
Essa abordagem simplificada de dosagem não leva em consideração outros fatores e pode resultar na administração de uma dose excessiva ou insuficiente de um medicamento ao paciente. Como resultado, alguns pacientes podem apresentar toxicidade desnecessária ou eficácia insuficiente da quimioterapia recebida.
Para melhorar a precisão da dosagem da quimioterapia, engenheiros do MIT desenvolveram uma abordagem alternativa que permite personalizar a dose para cada paciente. O sistema mede a quantidade de medicamento no corpo do paciente e insere esses dados em um controlador que pode ajustar a taxa de infusão de acordo.
Essa abordagem pode ajudar a compensar as diferenças na farmacocinética dos medicamentos causadas pela composição corporal, predisposição genética, toxicidade orgânica induzida pela quimioterapia, interações com outros medicamentos e alimentos e variações circadianas nas enzimas responsáveis pela degradação dos medicamentos quimioterápicos, dizem os pesquisadores.
"Ao reconhecer os avanços na compreensão de como os medicamentos são metabolizados e aplicar ferramentas de engenharia para simplificar a dosagem personalizada, acreditamos que podemos ajudar a transformar a segurança e a eficácia de muitos medicamentos", disse Giovanni Traverso, professor associado de engenharia mecânica no MIT, gastroenterologista no Brigham and Women's Hospital e autor sênior do estudo.
Louis DeRidder, estudante de pós-graduação do MIT, é o principal autor do artigo publicado no periódico Med.
Monitoramento contínuo
Neste estudo, os pesquisadores se concentraram em um medicamento chamado 5-fluorouracil, usado para tratar câncer colorretal e outros tipos de câncer. O medicamento é normalmente administrado ao longo de um período de 46 horas, e sua dosagem é determinada por meio de uma fórmula baseada na altura e no peso do paciente, o que fornece uma estimativa da área de superfície corporal.
No entanto, essa abordagem não leva em consideração as diferenças na composição corporal, que podem afetar a distribuição do medicamento no organismo, ou as variações genéticas que afetam a sua metabolização. Essas diferenças podem levar a efeitos colaterais prejudiciais se o medicamento for administrado em excesso. Se não for administrado em quantidade suficiente, o tumor pode não ser eliminado como esperado.
"Pessoas com a mesma área de superfície corporal podem ter alturas e pesos muito diferentes, massa muscular diferente ou genética diferente, mas, desde que a altura e o peso somados a essa equação resultem na mesma área de superfície corporal, a dose será idêntica", afirma DeRidder, candidato a doutorado no programa de engenharia médica e física médica do Programa Harvard-MIT em Ciências da Saúde e Tecnologia.
Outro fator que pode alterar a quantidade de fármaco no sangue a qualquer momento é a variação circadiana em uma enzima chamada di-hidropirimidina desidrogenase (DPD), que decompõe o 5-fluorouracil. A expressão da DPD, como muitas outras enzimas no corpo, é regulada por um ritmo circadiano. Portanto, a degradação do 5-FU pela DPD não é constante, mas varia com o horário do dia. Esses ritmos circadianos podem resultar em uma variação de dez vezes na quantidade de 5-FU no sangue de um paciente durante uma infusão.
"Usando a área de superfície corporal para calcular a dose de quimioterapia, sabemos que duas pessoas podem apresentar toxicidades muito diferentes ao 5-fluorouracil. Um paciente pode ter ciclos de tratamento com toxicidade mínima e, em seguida, um ciclo com toxicidade terrível. Algo mudou na maneira como o paciente metabolizou a quimioterapia de um ciclo para o outro. Nosso método de dosagem desatualizado não captura essas mudanças, e os pacientes sofrem como resultado", afirma Douglas Rubinson, oncologista clínico do Instituto de Câncer Dana-Farber e um dos autores do artigo.
Uma maneira de tentar compensar a variabilidade na farmacocinética da quimioterapia é uma estratégia chamada monitoramento terapêutico de medicamentos, na qual o paciente coleta uma amostra de sangue ao final de um ciclo de tratamento. Após a análise das concentrações do medicamento, a dosagem pode ser ajustada, se necessário, no início do próximo ciclo (geralmente duas semanas para 5-fluorouracil).
Foi demonstrado que essa abordagem leva a melhores resultados para os pacientes, mas não tem sido amplamente utilizada para quimioterapias como o 5-fluorouracil.
Os pesquisadores do MIT queriam desenvolver um tipo semelhante de monitoramento, mas de forma automatizada, que permitisse a personalização da dosagem de medicamentos em tempo real, o que poderia levar a melhores resultados para os pacientes.
Em seu sistema de circuito fechado, as concentrações do medicamento podem ser monitoradas continuamente e essas informações são usadas para ajustar automaticamente a taxa de infusão do medicamento quimioterápico para manter a dose dentro da faixa-alvo.
Esse sistema de circuito fechado permite que a dosagem do medicamento seja personalizada para levar em conta os ritmos circadianos dos níveis de enzimas metabolizadoras do medicamento, bem como quaisquer alterações na farmacocinética do paciente desde o último tratamento, como toxicidade orgânica induzida por quimioterapia.
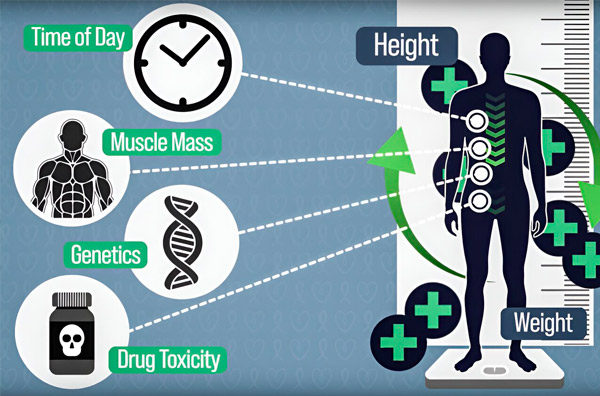
Para tornar a dosagem da quimioterapia mais precisa, engenheiros do MIT desenvolveram uma maneira de medir continuamente a quantidade de medicamento no corpo de um paciente durante uma infusão de várias horas. Isso ajudará a compensar as diferenças causadas pela composição corporal, genética, toxicidade do medicamento e oscilações circadianas. Fonte: Cortesia dos pesquisadores.
O novo sistema desenvolvido pelos pesquisadores, conhecido como CLAUDIA (Closed-Loop AUtomated Drug Infusion RegulAtor), utiliza equipamentos disponíveis comercialmente para cada etapa. Amostras de sangue são coletadas a cada cinco minutos e rapidamente preparadas para análise. A concentração de 5-fluorouracil no sangue é medida e comparada com a faixa-alvo.
A diferença entre as concentrações alvo e medidas é inserida em um algoritmo de controle, que então ajusta a taxa de infusão conforme necessário para manter a dose dentro da faixa de concentrações nas quais o medicamento é eficaz e não tóxico.
"Desenvolvemos um sistema no qual podemos medir continuamente a concentração do medicamento e ajustar a taxa de infusão adequadamente para manter a concentração do medicamento na janela terapêutica", diz DeRidder.
Ajuste rápido
Em testes com animais, os pesquisadores descobriram que, usando CLAUDIA, eles conseguiram manter a quantidade de medicamento circulando no corpo na faixa desejada em cerca de 45% do tempo.
Os níveis do fármaco em animais que receberam quimioterapia sem o tratamento com CLAUDIA permaneceram na faixa-alvo em apenas 13% das vezes, em média. Os pesquisadores não testaram a eficácia dos níveis do fármaco neste estudo, mas acredita-se que manter as concentrações na janela-alvo resulte em melhores resultados e menos toxicidade.
CLAUDIA também conseguiu manter a dose de 5-fluorouracil na faixa-alvo mesmo quando um medicamento que inibe a enzima DPD foi administrado. Em animais que receberam esse inibidor sem monitoramento e ajuste contínuos, os níveis de 5-fluorouracil aumentaram até oito vezes.
Para esta demonstração, os pesquisadores executaram manualmente cada etapa do processo usando equipamentos prontos para uso, mas agora planejam automatizar cada etapa para que o monitoramento e os ajustes de dose possam ser feitos sem intervenção humana.
Para medir as concentrações do fármaco, os pesquisadores usaram cromatografia líquida de alta eficiência com espectrometria de massas (HPLC-MS), uma técnica que pode ser adaptada para detectar quase qualquer tipo de fármaco.
"Vemos um futuro em que podemos usar CLAUDIA para qualquer medicamento que tenha as propriedades farmacocinéticas apropriadas e seja detectável por HPLC-MS, permitindo a dosagem personalizada para muitos medicamentos diferentes", diz DeRidder.
