Novas publicações
FDA aprova nova terapia para pacientes com glioma pela primeira vez em décadas
Última revisão: 02.07.2025

Todo o conteúdo do iLive é medicamente revisado ou verificado pelos fatos para garantir o máximo de precisão factual possível.
Temos diretrizes rigorosas de fornecimento e vinculamos apenas sites de mídia respeitáveis, instituições de pesquisa acadêmica e, sempre que possível, estudos médicos revisados por pares. Observe que os números entre parênteses ([1], [2], etc.) são links clicáveis para esses estudos.
Se você achar que algum dos nossos conteúdos é impreciso, desatualizado ou questionável, selecione-o e pressione Ctrl + Enter.
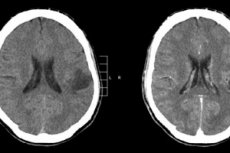
O vorasidenib foi aprovado pela Food and Drug Administration (FDA) dos EUA para pacientes com gliomas de grau 2 com mutações IDH1 ou IDH2.
Com base em dados do ensaio clínico INDIGO, um ensaio clínico global de fase III, duplo-cego e randomizado, o vorasidenibe mais que dobrou a sobrevida livre de progressão e retardou a necessidade de tratamento com radiação e quimioterapia em pacientes com glioma de grau 2 com mutação IDH após cirurgia de ressecção tumoral. O INDIGO foi o primeiro ensaio clínico de fase III de uma terapia direcionada para glioma com mutação IDH.
"O estudo INDIGO mostra que os inibidores de IDH podem funcionar em gliomas de baixo grau com mutação de IDH", afirma Patrick Wen, médico, diretor do Centro de Neuro-Oncologia do Instituto de Câncer Dana-Farber e um dos três coordenadores do estudo. "O último medicamento aprovado para gliomas de baixo grau foi aprovado em 1999, então este seria o primeiro medicamento novo em muito tempo."
Gliomas de grau 2 são tumores cerebrais incuráveis. Mutações no gene IDH são encontradas na grande maioria dos gliomas de baixo grau.
Um benefício fundamental da terapia com vorasidenibe é que ela pode retardar a necessidade de radioterapia e quimioterapia. O tratamento atual envolve cirurgia seguida de radioterapia e quimioterapia. Radioterapia e quimioterapia são tratamentos eficazes, mas após muitos anos de tratamento, os pacientes começam a apresentar sinais de disfunção cognitiva, tipicamente observados em pessoas muito mais velhas.
"Esses pacientes geralmente são jovens, na faixa dos 30 ou 40 anos. Mas, 10 a 20 anos depois, mesmo que estejam se recuperando bem do tumor, frequentemente apresentam sinais de demência após a radioterapia e a quimioterapia", diz Wen. "Se este medicamento puder retardar o início desses tratamentos, poderá retardar a disfunção cognitiva dos pacientes e preservar sua qualidade de vida."
O estudo INDIGO incluiu 331 pacientes com gliomas de grau 2 com mutação IDH que foram submetidos à cirurgia para remoção do tumor. Os pacientes incluídos no estudo não necessitaram de radioterapia ou quimioterapia imediata e estavam em período de acompanhamento. Durante esse período, foram randomizados para receber vorasidenibe ou placebo.
Os pacientes que tomaram vorasidenibe apresentaram sobrevida livre de progressão mediana de 27,7 meses, em comparação com 11,1 meses para os pacientes que tomaram placebo. O tempo até o próximo tratamento para os pacientes que tomaram placebo foi de 17,8 meses.
Em pacientes tratados com vorasidenibe, a mediana não foi determinada no momento da última análise, visto que apenas 11,3% desses pacientes haviam passado para o próximo tratamento até o momento. O medicamento também apresentou um perfil de segurança administrável.
"O estudo não encontrou diferença na qualidade de vida em comparação com o placebo", diz Wen. "A tolerabilidade é importante porque esperamos que as pessoas tomem este medicamento por muitos anos."
A aprovação abre diversas novas opções para os pacientes. Por exemplo, Van tem um estudo em andamento avaliando o vorasidenibe em combinação com imunoterapia, e estudos combinando o vorasidenibe com radiação e quimioterapia padrão estão sendo planejados.
