Novas publicações
IA detecta câncer de próstata em estágio inicial não detectado por patologistas
Última revisão: 23.08.2025

Todo o conteúdo do iLive é medicamente revisado ou verificado pelos fatos para garantir o máximo de precisão factual possível.
Temos diretrizes rigorosas de fornecimento e vinculamos apenas sites de mídia respeitáveis, instituições de pesquisa acadêmica e, sempre que possível, estudos médicos revisados por pares. Observe que os números entre parênteses ([1], [2], etc.) são links clicáveis para esses estudos.
Se você achar que algum dos nossos conteúdos é impreciso, desatualizado ou questionável, selecione-o e pressione Ctrl + Enter.
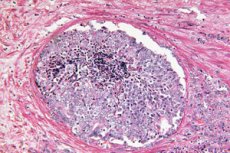
A Scientific Reports demonstra que a inteligência artificial consegue reconhecer pistas morfológicas ocultas de tumores em biópsias de próstata que antes eram consideradas benignas por um patologista. Um modelo de aprendizado profundo treinado com a abordagem de supervisão fraca previu quais homens com PSA elevado desenvolveriam câncer de próstata clinicamente significativo (ISUP > 1) nos próximos 30 meses e quais permaneceriam livres de câncer por pelo menos 8 anos. Isso abre caminho para a estratificação precoce de risco imediatamente após uma biópsia inicial "limpa" e pode ajudar a decidir quem realmente precisa de procedimentos invasivos repetidos e vigilância reforçada.
Contexto do estudo
A biópsia primária por agulha da próstata frequentemente produz resultados falso-negativos: uma proporção significativa de câncer clinicamente significativo permanece "fora do rastreio", especialmente com a biópsia TRUS sistemática tradicional. A introdução da orientação por ressonância magnética aumentou a proporção de detecção de câncer clinicamente significativo e reduziu o número de procedimentos repetidos desnecessários, mas mesmo com estratégias modernas, alguns tumores agressivos permanecem sem detecção. O dilema clínico permanece o mesmo: quem deve ser observado após uma biópsia "limpa" e quem deve ser encaminhado para uma biópsia repetida precocemente, para não atrasar o diagnóstico e não sobrecarregar os pacientes com intervenções invasivas.
A base biológica para a solução deste problema é o fenômeno TINT (tumor-instructed/indicating normal tissue): um tumor "reconfigura" os tecidos aparentemente normais circundantes do órgão, deixando neles traços fracos, mas sistemáticos – desde remodelação estromal e hipóxia até alterações metabólicas. Essas alterações foram descritas em modelos experimentais e em pacientes com câncer de próstata e se correlacionam com a agressividade do tumor, o que torna o tecido "normal" uma fonte potencial de sinais diagnósticos, mesmo que não haja glândulas cancerígenas óbvias no núcleo da biópsia.
Métodos de patologia digital e aprendizado profundo visam extrair essas características de campo "sutis" de cortes padrão de H&E. Diferentemente da morfologia clássica, que se concentra em estruturas tumorais óbvias, algoritmos podem capturar padrões distribuídos no estroma e epitélio associados à presença de um tumor em outra parte do órgão. Isso abre caminho para a estratificação de risco imediatamente após uma biópsia negativa: uma "pontuação" de vidro alta sugere a conveniência de uma repetição precoce da biópsia ou orientação por ressonância magnética, enquanto uma baixa sugere uma observação mais cuidadosa.
Esta é a ideia por trás de um novo estudo publicado na Scientific Reports: os autores testaram se a IA pode prever câncer de próstata clinicamente significativo nos próximos 30 meses com base em sinais morfológicos de biópsias TINT. O trabalho se baseia em uma pré-impressão apresentada anteriormente e forma uma base aplicada para a implementação de biomarcadores digitais de "campo" no encaminhamento de pacientes após uma biópsia inicial "limpa".
Como foi feito: design, dados, algoritmo
Os autores coletaram retrospectivamente uma coorte de 232 homens com PSA elevado e uma conclusão inicial de "benigno" na biópsia por agulha (após controle técnico, 213 pacientes e 587 cortes foram incluídos na análise final; biópsias de 1997 a 2016, Umea, Suécia). Cada paciente foi pareado com um par "espelho" por idade, ano de diagnóstico e nível de PSA: metade foi diagnosticada com câncer de próstata posteriormente (≤ 30 meses), a outra metade permaneceu livre de câncer por pelo menos 8 anos. As lâminas de H&E foram digitalizadas (20x), cortadas em blocos de 256x256 pixels e alimentadas no CLAM (Clustering-constrained Attention Multiple-Instance Learning) – um esquema moderno com supervisão fraca, em que apenas o destino do paciente é conhecido, e não a marcação de cada pixel. As características foram extraídas pelo ResNet18 pré-treinado em 57 conjuntos de dados histopatológicos. O ponto final é binário: baixo risco (benigno/ISUP1) vs. alto risco (ISUP2-5).
Precisão da previsão
Em um teste independente, o modelo atingiu uma AUC de 0,81 em todas as lâminas e uma AUC de 0,82 no nível do paciente. Em um limiar que proporcionou um equilíbrio aceitável, a sensibilidade foi de 0,92, com uma taxa de falsos positivos de 0,32 (nível do paciente). Em outras palavras, entre as pessoas cuja biópsia inicial "falhou", a IA sinalizou corretamente a grande maioria daquelas que logo foram confirmadas como portadoras de câncer clinicamente significativo, embora ao custo de alguns alarmes falsos. Para a clínica, isso é um sinal: resposta "benigna" da biópsia ≠ risco zero, e pode ser estratificada quantitativamente por lentes digitais.
O que exatamente a IA “percebe” em tecido “normal”?
A interpretação via UMAP e mapas de atenção mostrou que as alterações estromais são as mais informativas:
- Mais colágeno no estroma (compactação da matriz, “fibrose”);
- Menos células musculares lisas ao redor das glândulas;
- Menos comuns são os sinais sutis no epitélio glandular, provavelmente abaixo da resolução de subamostragem disponível.
Esse padrão se enquadra no conceito TINT (tumor-instructed/indicating normal tissue): até mesmo a "norma" em um órgão onde um tumor está oculto é reconfigurada sob sua influência e difere da "norma" em um órgão sem tumor. O câncer não é apenas um ninho, mas também um campo, e a IA aprende a ler o efeito de campo.
Como a abordagem é útil na prática - cenários potenciais
- Rebiópsia baseada em risco: alta taxa de IA em vidro "limpo" - argumento a favor da rebiópsia precoce ou orientação por ressonância magnética em vez de esperar.
- Personalização do monitoramento: a baixa velocidade contrabalança a ansiedade após a ressonância magnética “limítrofe” e permite a moderação da intensidade do monitoramento.
- Treinamento do padrão TINT: mapas de atenção e sobreposições interativas ajudam os patologistas a ver campos sutis ao redor do câncer, melhorando a consistência dos relatórios.
É importante entender as limitações
Trata-se de um centro único no norte da Suécia (população predominantemente caucasiana), o desenho é retrospectivo, as biópsias basais foram realizadas sem orientação por ressonância magnética (biópsias TRUS sistemáticas) e os marcadores são resultados futuros, em vez de "tumor oculto na mesma lâmina". Ainda não há validação externa em centros/scanners independentes, nem um estudo prospectivo sobre o efeito do algoritmo nas decisões e resultados clínicos. A taxa de falsos positivos permanece significativa — o modelo não substitui o médico, mas adiciona uma camada probabilística para a tomada de decisão compartilhada.
O que vem a seguir: Roteiro de implementação
- Validação externa multicêntrica (diferentes scanners, protocolos, grupos étnicos).
- Estudos de decisão prospectiva: a pontuação da IA altera a trajetória do paciente (tempo até o diagnóstico, número de biópsias repetidas desnecessárias, sobrediagnóstico/subdiagnóstico).
- Integração com ressonância magnética e clínica: modelos combinados (PSA, PIRADS de ressonância magnética, fatores clínicos + pontuação TINT de acordo com H&E).
- Etapas técnicas: padronização da digitalização, controle do desvio de dados, explicabilidade (sobreposições de atenção para rotina).
Fonte: Chelebian E., Avenel C., Järemo H., Andersson P., Bergh A., Wählby C. et al. Descoberta de tumor que indica alterações morfológicas em biópsias benignas de próstata por meio de IA. Scientific Reports (Nature Portfolio), publicado em 21 de agosto de 2025. DOI: https://doi.org/10.1038/s41598-025-15105-6
